题目内容
【题目】设NA为阿伏加德罗常数的值。下列有关叙述正确的是
A. 标准状况下,向2.24L密闭容器中充满NO2气体,其所含分子数为0.1 NA
B. CuO和Cu2S的混合物80 g中,所含铜粒子数为2NA
C. 常温常压下,22gT2O含中子数为12NA
D. 1.0 L 1.0 mol·L-1的NaNO3水溶液中含有的氧原子数为3NA
【答案】C
【解析】分析:A、根据NO2与N2O4存在平衡关系解答;
B、根据CuO和Cu2S的组成分析;
C、T2O含有12个中子,结合n=m÷M解答;
D、溶剂水中还含有氧原子。
详解:A、标准状况下,向2.24L密闭容器中充满NO2气体,由于存在:2NO2![]() N2O4,因此其所含分子数小于0.1 NA,A错误;
N2O4,因此其所含分子数小于0.1 NA,A错误;
B、CuO、Cu2S中铜元素的百分含量均是80%,所以二者组成的混合物80 g中,所含铜粒子数为![]() NA,B错误;
NA,B错误;
C、常温常压下,22gT2O的物质的量是![]() =1mol,因此所含中子数为12NA,C正确;
=1mol,因此所含中子数为12NA,C正确;
D、1.0 L 1.0 mol·L-1的NaNO3水溶液中硝酸钠的物质的量是1mol,其中含有的氧原子数为3NA,但溶剂水中还含有大量的氧原子,D错误。答案选C。

 名校课堂系列答案
名校课堂系列答案【题目】25℃时,有关物质的电离平衡常数如下:
化学式 | CH3COOH | H2CO3 | H2SO3 |
电离平衡常数 | K=1.8×10-5 | K1=4.3×10-7 K2=5.6×10-11 | K1=1.5×10-2 K2=1.02×10-7 |
(1)请写出H2SO3的电离平衡常数K1的表达式:________________。
(2) 常温下,将体积为10mL pH=2的醋酸溶液与亚硫酸溶液分别加蒸馏水稀释至1000mL,稀释后溶液的pH,前者_____后者(填“>”、“<”或“=”)。
(3)一定条件下,冰醋酸加水稀释过程中溶液导电能力I随加水体积V变化曲线如右图所示,则a、b、c三点溶液醋酸的电离程度由大到小为____________________。

(4)下列离子CH3COO-、CO32-、HSO3-、SO32-在溶液中结合H+的能力由大到小的关系为___________。
(5)体积相同、c(H+)相同的①CH3COOH;②HCl;③H2SO4 三种酸溶液分别与同浓度的NaOH溶液完全中和时,消耗NaOH溶液的体积由大到小的排列顺序是_____(填序号)。
(6)已知,H+(aq) + OH-(aq) == H2O(l) ΔH =-57.3 kJ/mol。实验测得稀醋酸与稀NaOH溶液反应生成1 mol H2O时放出57 kJ的热,则醋酸溶液中,醋酸电离的热化学方程式为________________。
【题目】锗是一种重要的半导体材料。工业上用精硫锗矿(主要成分为GeS2,杂质不反应)制取Ge,其工艺流程如图所示:
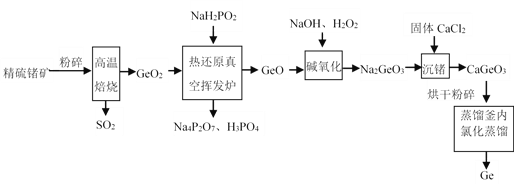
回答下列问题:
(1)开始将精硫锗矿粉碎的目的是______。
(2)高温焙烧精硫锗矿的化学方程式为______。
(3)热还原真空挥发炉内反应的化学方程式为______。
(4)在沉锗过程中,当温度为90℃,pH为14时,加料量(CaCl2/Ge质量比)对沉锗的影响如表所示,选择最佳加料量为______(填“10-15”“15-20”或“20-25”),理由是______。
编号 | 加料量(CaCl2/Ge) | 母液体积 (mL) | 过滤后液含锗(mg/L) | 过滤后液 pH | 锗沉淀率(%) |
1 | 10 | 500 | 76 | 8 | 93.67 |
2 | 15 | 500 | 20 | 8 | 98.15 |
3 | 20 | 500 | 2 | 11 | 99.78 |
4 | 25 | 500 | 1.5 | 12 | 99.85 |
(5)某温度时,沉锗得到的CaGeO3在水中的沉淀溶解平衡曲线如图所示。下列说法错误的是______。
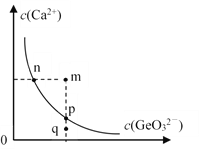
a.n点与p点对应的Ksp相等
b.通过蒸发可以使溶液由q点变到p点
c.q点无CaGeO3沉淀生成
d.加入Na2GeO3可以使溶液由n点变到m点
(6)CaGeO3与强酸反应可得到H2GeO3。0.l molL-1的NaHGeO3溶液pH_____(填“>”“=”或“<”)7,判断理由是______(通过计算比较)。(25℃时,H2GeO3的Ka1=1.7×10-9,Ka2=1.9×10-13。)