题目内容
【题目】镁是一种银白色的碱土金属,镁元素在地壳中的含量约为2.00%,位居第八位,镁及其化合物在研究和生产中具有广泛用途。请回答下列问题:
(1)氮化镁(Mg3N2)是由氮和镁所组成的无机化合物。在室温下纯净的氮化镁为黄绿色的粉末,能与水反应,常用作触媒,实验室欲用如图1所示装置和药品制备少量氮化镁。

①A中盛装的是浓氨水,B中可盛装___,二者混合可制取氨气。
②按照气流的方向从左至右连接装置:a接___、___接___、___接___。
③已知氨气有还原性,能还原氧化铜,生成物之一是空气的主要成分,该反应的化学方程式为____________________。
④如果没有装有无水氯化钙的装置,可能发生反应的化学方程式为____________________。
(2)碳酸镁可用作耐火材料、锅炉和管道的保温材料,以及食品、药品、化妆品、橡胶、墨水等的添加剂。合成碳酸镁晶须的步骤如下:
步骤1:配制0.5 mol·L-1 MgSO4溶液和0.5 mol·L-1 NH4HCO3溶液。
步骤2:用量筒量取500 mL NH4HCO3溶液于1 000 mL四口烧瓶中,开启搅拌器,温度控制在50 ℃。
步骤3:将250 mL MgSO4溶液逐滴加入NH4HCO3溶液中,1 min内滴加完毕,然后用氨水调节溶液pH到9.5。
步骤4:放置1 h后,过滤,洗涤。
步骤5:在40 ℃的真空干燥箱中干燥10 h,得到碳酸镁晶须产品(MgCO3·nH2O,n=1~5)。
①配制0.5 mol·L-1 MgSO4溶液500 mL,需要的仪器有托盘天平、药匙、烧杯、玻璃棒、量筒、胶头滴管、_____。
②步骤3中加氨水后反应的离子方程式为______________。
测定合成的MgCO3·nH2O中的n值。
称量1.000 g碳酸镁晶须,放入图2所示的广口瓶中,加入适量水,滴入稀硫酸与晶须反应,生成的CO2被NaOH溶液吸收,在室温下反应4~5 h,后期将温度升到30 ℃,最后烧杯中的溶液用已知浓度的盐酸滴定,测得生成CO2的总量;重复上述操作2次。
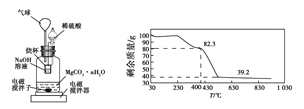
③图中气球的作用是__________________。
④上述反应后期要升温到30 ℃,主要目的是________________。
⑤若实验测得1.000 g碳酸镁晶须产生CO2的平均物质的量为a mol,则n为___(用含a的表达式表示)。
⑥称取100 g上述晶须产品进行热重分析,得到的热重曲线如图所示,则合成的晶须中n=______。
【答案】生石灰或氢氧化钠 d e c b f 2NH3+3CuO ![]() N2+3H2O+3Cu Mg3N2+6H2O
N2+3H2O+3Cu Mg3N2+6H2O![]() 3Mg(OH)2+2NH3↑ 500 mL容量瓶 Mg2++HCO3-HCO3-+NH3·H2O+(n-1)H2O
3Mg(OH)2+2NH3↑ 500 mL容量瓶 Mg2++HCO3-HCO3-+NH3·H2O+(n-1)H2O![]() MgCO3·nH2O↓+NH4+ 暂时储存CO2,有利于CO2被NaOH溶液吸收,且能保持装置中压强相对稳定 升高温度气体的溶解度减小,使溶解在水中的CO2逸出,便于吸收完全
MgCO3·nH2O↓+NH4+ 暂时储存CO2,有利于CO2被NaOH溶液吸收,且能保持装置中压强相对稳定 升高温度气体的溶解度减小,使溶解在水中的CO2逸出,便于吸收完全 ![]() 1
1
【解析】
(1)①浓氨水和生石灰或氢氧化钠固体混合放热,使一水合氨分解生成氨气,故答案为:
②根据实验目的及题给装置可知,按照气流的方向从左向右连接装置的顺序为:a接d,e接c,b接f,故答案为:
③氨气有还原性,能还原氧化铜,生成物之一是空气的主要成分氮气,则氨气与氧化铜反应的化学方程式为:2NH3+3CuO![]() N2+3H2O+3Cu,故答案为:d;e;c;b;f;
N2+3H2O+3Cu,故答案为:d;e;c;b;f;
④氮化镁能和水发生反应生成氢氧化镁和氨气,化学方程式为:Mg3N2+6H2O=3Mg(OH)2
+2NH3↑,故答案为:Mg3N2+6H2O=3Mg(OH)2+2NH3↑;
(2)①配制0.5 mol·L-1 MgSO4溶液500 mL,除提供的仪器外,还需要的仪器为500 mL容量瓶,故答案为:500 mL容量瓶;
②步骤3中加氨水后反应生成碳酸镁结晶水合物,反应的离子方程式为Mg2++HCO3—+NH3·H2O+(n-1)H2O=MgCO3·nH2O↓+NH4+,故答案为:Mg2++HCO3—+NH3·H2O+(n-1)H2O=
MgCO3·nH2O↓+NH4+;
③题图2装置中气球可以暂时储存CO2,有利于CO2被NaOH溶液吸收,且能保持装置中压强相对稳定,故答案为:暂时储存CO2,有利于CO2被NaOH溶液吸收,且能保持装置中压强相对稳定;
④题述反应后期将温度升到30 ℃,是为了使生成的二氧化碳全部逸出,便于其被氢氧化钠溶液完全吸收,从而减小测定产生的误差,故答案为:升高温度气体的溶解度减小,使溶解在水中的CO2逸出,便于吸收完全;
⑤若实验测得1.000 g碳酸镁晶须产生的CO2的平均物质的量为a mol,依据碳元素守恒可知,晶须中碳酸镁的物质的量为a mol,根据MgCO3·nH2O中碳酸镁和结晶水的物质的量之比为1∶n,得到1∶n=a∶![]()
![]() ,得到n=
,得到n=![]()
![]() ,故答案为:
,故答案为:![]() ;
;
⑥由题图3知400 ℃时剩余质量为82.3 g,这是该晶须失去结晶水后的质量,则有100×![]()
![]() =100-82.3,解得n=1,故答案:1。
=100-82.3,解得n=1,故答案:1。

 导学与测试系列答案
导学与测试系列答案 新非凡教辅冲刺100分系列答案
新非凡教辅冲刺100分系列答案