题目内容
【题目】部分氧化的 Fe-Cu 合金样品(氧化物为 Fe2O3、CuO)共5.76 g,经如下处理:

下列说法正确的是( )
A. 滤液A中的阳离子为Fe2+、Fe3+、H+ B. 溶解样品消耗的硫酸共为 0.04 mol
C. 样品中氧元素的质量为 0.48 g D. V=336 mL
【答案】B
【解析】
硫酸足量可以说明沉淀中无Fe、CuO、Fe2O3,溶液无铜离子可以说明铜都析出了,滤渣3.2g一定是全部的铜;最后灼烧得到固体3.2g为Fe2O3,其中含铁元素质量为3.2×112/160=2.24g,部分氧化的 Fe-Cu 合金样品中铁元素质量为2.24 g,铜元素的质量为3.2g,则氧元素质量为5.76-2.24—3.2g =0.32g;由于最后溶液中溶质为过量H2SO4和FeSO4,而铁元素物质的量为2.24/56=0.04mol,说明参加反应硫酸物质的量为0.04mol;参加反应硫酸电离出的与H+部分氢离子生成氢气,另外的H+和合金中的氧结合成水了,计算合金中氧原子的物质的量,进而计算氧原子它结合氢离子物质的量,再根据H原子守恒生成氢气的体积。
生成的滤渣3.2g是铜,金属铜可以和三价铁反应,所以一定不含有三价铁离子,A错误;根于最后溶液中溶质为过量H2SO4和FeSO4,而铁元素物质的量为0.04mol,说明参加反应硫酸物质的量为0.04mol,B正确;最后灼烧得到固体3.2g为Fe2O3,其中含铁元素质量为3.2×112/160=2.24g,部分氧化的 Fe-Cu 合金样品中铁元素质量为2.24 g,铜元素的质量为3.2g,则氧元素质量为5.76-2.24—3.2g =0.32g,C错误;0.04mol硫酸电离出氢离子0.08mol,其中部分氢离子生成氢气,另外的H+和合金中的氧结合成水了,由于合金中氧元素质量为为3.2g.氧的物质的量0.02mol,它结合氢离子0.04mol,所以硫酸中有0.08-0.04=0.04molH+生成氢气,即生成0.02mol氢气,标况体积为448ml,D错误。

【题目】下表为元素周期表的一部分,请参照元素①-⑧在表中的位置,用化学用语回答下列问题:
族 周期 | IA | 0 | ||||||
1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
2 | ② | ③ | ④ | |||||
3 | ⑤ | ⑥ | ⑦ | ⑧ | ||||
(1)④、⑤、⑥的原子半径由大到小的顺序为_____________________(填化学式)。
(2)②、③、⑦的最高价含氧酸的酸性由强到弱的顺序是___________。
(3)①、④、⑤、⑧中的某些元素可形成既含离子键又含极性共价键的化合物,写出其中一种化合物的电子式:_______。
(4)由表中两种元素的原子按1:1组成的常见液态化合物的溶液易被催化分解,写出其化学方程式____。
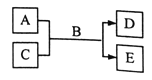
(5)由表中元素形成的常见物质X、Y、Z、M、N可发生以下反应:

X溶液与Y溶液反应的离子方程式为_____________,N→⑥的单质的化学方程式为_____________。
【题目】在四支试管中,在不同条件下发生反应:Fe+2HCl = FeCl2+H2↑,判断产生H2的反应速率最快的是:
试管 | 盐酸浓度 | 温度 | 铁的状态 |
① | 0.5 mol·L-1 | 20 ℃ | 块状 |
② | 0.5 mol·L-1 | 20 ℃ | 粉末状 |
③ | 1 mol·L-1 | 35 ℃ | 块状 |
④ | 2 mol·L-1 | 35 ℃ | 粉末状 |
A. ① B. ② C. ③ D. ④