��Ŀ����
�� ��֪��2CO2(g)+6H2(g) ![]() CH3CH2OH(g)+3H2O(g) ��ijЩ��ѧ���ļ����������±���
CH3CH2OH(g)+3H2O(g) ��ijЩ��ѧ���ļ����������±���
| ��ѧ�� | C��C | C��H | H��H | C��O | C=O | H��O |
| ����/kJ��mol-1 | 348 | 413 | 436 | 358 | 750 | 463 |
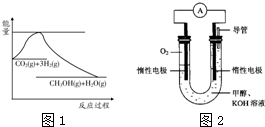
 ��Ӧ��CO2(g)+3H2(g)
��Ӧ��CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g)���ʱ��H=_______________________����S_____0(��>��<��=)
CH3OH(g)+H2O(g)���ʱ��H=_______________________����S_____0(��>��<��=)
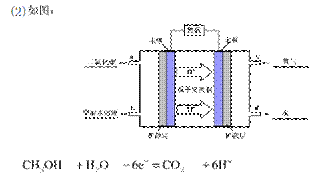
�� �״�-����ȼ�ϵ�أ�DMFC����һ�ָ�Ч�ܡ�����Ⱦ�綯�����ij��ص�أ���ȼ�ϵ�صĵ�ط�ӦʽΪ��CH3OH(l)��![]() O2(g) == CO2(g)��2H2O(l)���乤��ԭ��ʾ��ͼ���£�
O2(g) == CO2(g)��2H2O(l)���乤��ԭ��ʾ��ͼ���£�
����ͼ�ĺ����ϱ��a��b��c��d�ĸ������ͨ����ų����������ƣ���ѧʽ��
�����ĵ缫��ӦʽΪ ��
����25���£���a mol��L-1�İ�ˮ��0.01 mol��L-1������������ϣ���Ӧʱ��Һ��
c(NH4��)=c(Cl��)������Һ�� �ԣ���ᡱ��������С������ú�a�Ĵ���ʽ��ʾNH3��H2O�ĵ��볣��Kb= ��
�� -178 kJ��mol-1 <
���� ![]() mol��L-1 (2��)
mol��L-1 (2��)

��ϰ��ϵ�д�
�����Ŀ
 ��2012?ͨ����һģ��Ϊ���������ܼ��š��͡���̼���á������ʹ�����CO2�ĺ�������Ч�ؿ�������CO2����ѧ�������о���ν�CO2ת��Ϊ�����õ���Դ��Ŀǰ��ҵ����һ�ַ�������CO2������ȼ�ϼ״���һ�������·�����Ӧ��
��2012?ͨ����һģ��Ϊ���������ܼ��š��͡���̼���á������ʹ�����CO2�ĺ�������Ч�ؿ�������CO2����ѧ�������о���ν�CO2ת��Ϊ�����õ���Դ��Ŀǰ��ҵ����һ�ַ�������CO2������ȼ�ϼ״���һ�������·�����Ӧ��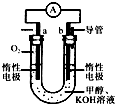 �״���Դ�ḻ���۸�������������淽�㣬��һ����Ҫ�Ļ���ԭ�ϣ�������Ҫ����;��Ӧ��ǰ����
�״���Դ�ḻ���۸�������������淽�㣬��һ����Ҫ�Ļ���ԭ�ϣ�������Ҫ����;��Ӧ��ǰ����