题目内容
过氧化氢是一种无色透明的无毒液体,是重要无机化工产品。试探究下列问题
(1)过氧化氢最适合贴上的一个标签是 。
|

(2)过氧化氢的制备方法很多,下列方法中原子利用率最高的是: 。
A. BaO 2 + H2SO 4 === BaSO4 ↓ + H2O2
B. 2NH4HSO4![]() (NH4)2S2O8 + H2↑,
(NH4)2S2O8 + H2↑,
然后水解 (NH4)2S2O8 + 2H2O =2NH4HSO4 + H2O2。
C.CH3CHOHCH3+O2→CH3COCH3+H2O2
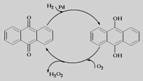
D.乙基蒽醌法:
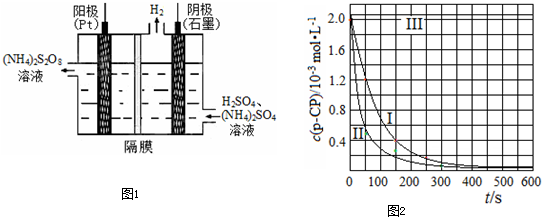
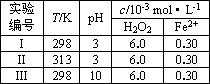
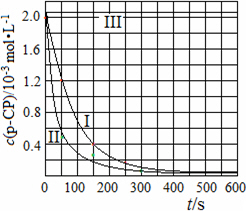
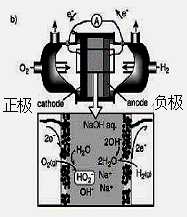
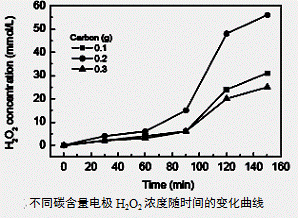
(3)碱性氢氧燃料电池工作时可产生过氧化氢(见下左图),正极含碳(Carbon)的质量大小对产生过氧化氢的浓度(concentration)有影响(其影响曲线如下右图)。
下列说法正确的有 。
A.开始时速率均较慢,说明电极有一个活化的过程
B.一段时间后,速率又再次平缓,说明生成与分解逐渐趋向平衡
C.正极室流出液经酸化后可分离出过氧化氢
D.正极含碳的质量以0.2g适宜
(4)过氧化氢作为一种绿色氧化剂有广泛应用,请写出下列反应的化学方程式:
①在过氧化氢作用下,铜与稀硫酸制硫酸铜: 。
②用Ti-Si分子筛作催化剂,甲苯被过氧化氢氧化为间-甲苯酚: 。
(1)B(2)D(3)ABCD (4)①Cu+H2SO4+H2O2=CuSO4+2H2O;
②H2O2 +![]()
![]()
![]() +H2O;
+H2O;
解析:
本题考查过氧化氢的制备。(2)D选项的物质可以循环利用,原子利用率最高;(3)从曲线可以看出,0~90minH2O2含量不高,90min后增大较快,A选项正确;120min后,生成速率减慢,说明生成与分解逐渐趋向平衡,B选项正确;正极反应为:H2O+O2+2e-=HO2-+OH-,生成的HO2-结合H+后产生H2O2,C选项正确;从三个曲线比较来看,正极含碳的质量0.2g时,H2O2的产率最高,D选项正确。(4)H2O2作为强氧化剂。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案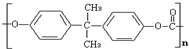 上海世博会于2010年5月1日开幕,本次世博会将以“绿色、低碳、节能、减排”为理念来选取材料设计展馆,上海企业联合馆的外围立面材料采用了聚碳酸酯透明塑料(如图),该材料是一种无色透明的无定性热塑性材料.其名称来源于其内部的CO3基团. 化学名:2,2'-双(4-羟基苯基)丙烷聚碳酸酯.下列关于聚碳酸酯的说法正确的( )
上海世博会于2010年5月1日开幕,本次世博会将以“绿色、低碳、节能、减排”为理念来选取材料设计展馆,上海企业联合馆的外围立面材料采用了聚碳酸酯透明塑料(如图),该材料是一种无色透明的无定性热塑性材料.其名称来源于其内部的CO3基团. 化学名:2,2'-双(4-羟基苯基)丙烷聚碳酸酯.下列关于聚碳酸酯的说法正确的( )| A、其单体是苯的同系物 | B、由单体合成聚碳酸酯属加聚反应 | C、该高分子化合物易溶于水 | D、没有固定的熔沸点 |