题目内容
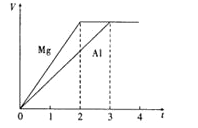
【题目】镁和铝分别与等浓度、等体积的过量稀硫酸反应,产生气体的体积(V)与时间(t)的关系如下图所示。反应中镁和铝的
A.摩尔质量之比为2∶3B.失去的电子数之比为8∶9
C.反应速率之比为2:3D.质量之比为4∶3
【答案】D
【解析】
A.摩尔质量以g/mol为单位,与其相对原子质量数值上相等,所以镁铝的摩尔质量之比为8:9,故A错误;
B.由图象可知,两个反应中生成的氢气一样多,说明两种金属提供的电子数目一样多,则失去的电子数之比为1:1,故B错误;
C.由图象可知,镁、铝与硫酸反应需要的时间之比为2:3,则二者的速率之比为3:2,故C错误;
D.由图象可知,两个反应中生成的氢气一样多,则镁、铝的物质的量之比为3:2,质量之比为(3×24):(2×27)=4:3,故D正确;
故答案为:D。

 阅读快车系列答案
阅读快车系列答案【题目】臭氧是一种强氧化剂,常用于消毒、灭菌等。
(1)O3与KI溶液反应生成的两种单质是______________和________________(填分子式)。
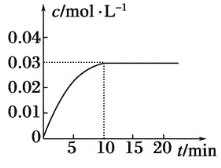
(2)O3在水中易分解,一定条件下,O3的浓度减少一半所需的时间(t)如下表所示。已知:O3的起始浓度为0.0216 mol/L。
T/℃ | 3.0 | 4.0 | 5.0 | 6.0 |
20 | 301 | 231 | 169 | 58 |
30 | 158 | 108 | 48 | 15 |
50 | 31 | 26 | 15 | 7 |
①pH增大能加速O3分解,表明对O3分解起催化作用的是________。
②在30 ℃、pH=4.0条件下,O3的分解速率为________mol/(L·min)。
③据表中的递变规律,推测O3在下列条件下分解速率依次增大的顺序为________(填字母代号)。
a.40 ℃、pH=3.0
b.10 ℃、pH=4.0
c.30 ℃、pH=7.0
【题目】一定条件下,通过下列反应可以制备特种陶瓷的原料MgO:MgSO4(s)+CO(g)MgO(s)+CO2(g)+SO2(g) ΔH>0。该反应在恒容密闭容器中达到平衡后,若仅改变图中横轴x的值,纵轴y随x变化趋势合理的是( )
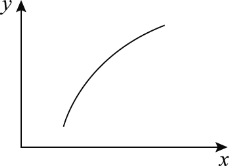
选项 | x | y |
A | CO的物质的量 | CO2与CO的物质的量之比 |
B | 反应温度 | 逆反应速率 |
C | 体系压强 | 平衡常数K |
D | MgSO4的质量(忽略体积) | CO的转化率 |
A.AB.BC.CD.D