题目内容
【题目】某化学兴趣小组为了探究常温下某非金属氧化物形成的未知气体的成分,将气体通入澄清石灰水,发现澄清石灰水变浑浊,持续通入发现浑浊又变澄清,由此该小组成员对气体的成分提出猜想。
[提出猜想]
猜想1:该气体为CO2;
猜想2:该气体为SO2;
猜想3:_________________________________________。
为了验证猜想,该小组设计实验加以探究:
[实验探究]该小组同学按如图所示装置,将气体从a端通入,则
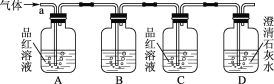
(1)B中应该装下列________试剂(填编号)。
A.NaCl溶液 B.酸性KMnO4溶液 C.盐酸 D.澄清石灰水
(2)A中品红溶液的作用是____________________________________。
(3)D中澄清石灰水的作用是________________________________________。
通过该实验,该小组同学观察到以下三个实验现象:①A中品红溶液褪色;②C中品红溶液不褪色;③D中澄清石灰水变浑浊,由上述现象该小组同学确认该气体的成分为________________。
【答案】该气体为CO2和SO2的混合气体 B 检验混合气体中是否含有SO2 检验混合气体中是否含有CO2 CO2和SO2的混合气体
【解析】
根据猜想1和猜想2,得出猜想3:该气体是CO2和SO2的混合气体;根据二氧化碳和二氧化硫的性质差异结合装置图以及题干中的问题分析解答,注意排除二氧化硫对二氧化碳检验的干扰。
根据猜想1和猜想2,得出猜想3:该气体是CO2和SO2的混合气体;
(1)SO2、CO2都能使澄清石灰水变浑浊,SO2能使品红溶液褪色,CO2不能使品红溶液褪色,因此先验证SO2的存在,通过品红溶液,如果品红溶液褪色,说明含有SO2,否则不含,然后利用SO2的还原性,用氧化剂除去SO2,可通过酸性高锰酸钾溶液或溴水,然后再通过品红溶液,检验SO2是否完全除尽,最后通入澄清石灰水,因此B装置应盛放酸性高锰酸钾溶液,答案选B;
(2)SO2能使品红溶液褪色,则A中品红溶液的作用是检验混合气体中是否含有SO2;
(3)CO2能使澄清石灰水变浑浊,则D中澄清石灰水的作用是检验原混合气体中是否含有CO2;
(4)①A中品红溶液褪色,说明原气体中含有SO2,②中品红溶液不褪色,说明SO2完全被除去,③D中澄清石灰水变浑浊,说明原气体中含有CO2,因此该气体的成分是SO2和CO2的混合气体。

 冲刺100分单元优化练考卷系列答案
冲刺100分单元优化练考卷系列答案