题目内容
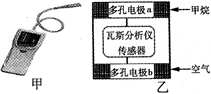
甲醇、氧气和强碱溶液做电解质的手机电池中的反应为:
2CH3OH+3O2+4OH-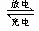 2CO32-+6H2O,有关说法正确的是
2CO32-+6H2O,有关说法正确的是
2CH3OH+3O2+4OH-
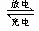 2CO32-+6H2O,有关说法正确的是
2CO32-+6H2O,有关说法正确的是 | A.放电时,CH3OH参与反应的电极为正极 |
| B.放电时,负极电极反应:CH3OH+8OH--6e- =CO32-+6H2O |
| C.标况下,通入11.2LO2完全反应有1mol电子转移 |
| D.充电时电解质溶液的pH逐渐减小 |
B
试题分析:A、放电时,CH3OH发生氧化反应,所以CH3OH参与反应的电极为负极,错误;B、放电时,负极为甲醇的氧化反应,结合电解质溶液,反应式为CH3OH+8OH--6e- =CO32-+6H2O,正确;C、标况下,11.2LO2的物质的量为0.5mol,所以11.2LO2完全反应有0.5mol×4=2mol电子转移,错误;D、充电时,反应从右向左进行,氢氧根离子浓度增大,溶液pH逐渐升高,错误,答案选B。

练习册系列答案
相关题目

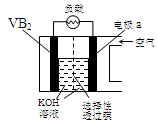
 2PbSO4+ 2H2O,根据此反应判断下列叙述中正确的是( )
2PbSO4+ 2H2O,根据此反应判断下列叙述中正确的是( )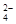 – 2e – = PbSO4
– 2e – = PbSO4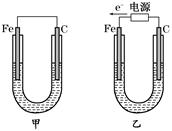
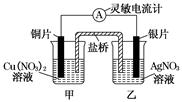
 CuSO4+H2↑
CuSO4+H2↑