题目内容
【题目】人们应用原电池原理制作了多种电池,以满足不同的需要.以下每小题中的电池广泛使用于日常生活、生产和科学技术等方面,请根据题中提供的信息,填写空格。
(1)铅蓄电池在放电时发生的电池反应式为:Pb+PbO2+2H2SO4═2PbSO4+2H2O。正极电极反应式为__,随着反应的进行,正极附近溶液的酸性将__。
(2)FeCl3溶液常用于腐蚀印刷电路铜板,发生2FeCl3+Cu═2FeCl2+CuCl2,若将此反应设计成原电池,则负极所用电极材料为__,当线路中转移0.4mol电子时,则被腐蚀铜的质量为__g。
(3)将铝片和铜片用导线相连,一组插入浓硝酸中,一组插入烧碱溶液中,分别形成了原电池,在这两个原电池中,负极分别为__。
A.铝片、铜片 B.铜片、铝片 C.铝片、铝片 D.铜片、铜片
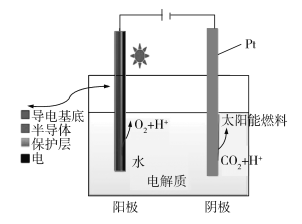
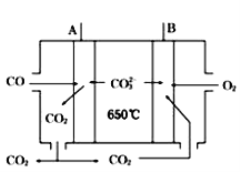
(4)如图是一种新型燃料电池,以CO为燃料,一定比例的Li2CO3和Na2CO3的熔融混合物为电解质,A极为电源(填“正”或“负”)___极,写出A极的电极反应式:___。
【答案】PbO2+4H++SO42-+2e-═PbSO4+2H2O 减弱 Cu 12.8 B 负极 CO-2e-+ CO32- =2CO2
【解析】
(1)铅蓄电池在放电时为原电池,正极发生还原反应,化合价降低;
(2)从化学方程式可知,铜的化合价升高,应该做负极,通过化学方程式知,每转移2mol电子,消耗1mol铜;
(3)插入浓硝酸中,因为铝与浓硝酸发生钝化反应,后续反应是铜和浓硝酸的反应;插入到氢氧化钠溶液,铝与氢氧化钠溶液发生氧化还原反应,铜不与氢氧化钠溶液反应;
(4)根据燃料电池的特点,通入燃料的一极为负极,通入氧气(或空气)的一极为正极。
(1)铅蓄电池在放电时发生的电池反应式为:Pb+PbO2+2H2SO4═2PbSO4+2H2O;正极发生还原反应,化合价降低,故正极的反应式为PbO2+4H++SO42-+2e-=PbSO4+2H2O,根据正极反应可知,随着反应的进行,氢离子被消耗,溶液的酸性减弱;
(2)根据原电池的工作原理,负极上失去电子,发生氧化反应,根据化合价变化,Cu的化合价升高,即负极材料是Cu,电极反应式为Cu-2e-=Cu2+,根据电极反应可知,每转移2mol电子,消耗1mol铜,则当线路中转移0.4mol电子时,则被腐蚀铜的质量为![]() ×64g/mol=12.8g;
×64g/mol=12.8g;
(3)插入浓硝酸中,因为铝与浓硝酸发生钝化反应,铜和浓硝酸发生氧化还原反应,即铜作负极;插入到氢氧化钠溶液,铝与氢氧化钠溶液发生氧化还原反应,铜不与氢氧化钠溶液反应,因此铝作负极,故答案选B;
(4)根据燃料电池的特点,通入燃料的一极为负极,通入氧气(或空气)的一极为正极,CO为燃料,则通入CO的一极为负极,即A极为负极,B为正极,Li2CO3和Na2CO3的熔融混合物为电解质,结合图示,则A极的电极反应式:CO-2e-+CO32-=2CO2。

 培优口算题卡系列答案
培优口算题卡系列答案 开心口算题卡系列答案
开心口算题卡系列答案 口算题卡河北少年儿童出版社系列答案
口算题卡河北少年儿童出版社系列答案【题目】下列反应属于氧化还原反应的是( )
A. SO3+ H2O= H2SO4 B. NH4Cl ![]() NH3
NH3![]() +HCl
+HCl![]()
C. Fe+CuSO4= FeSO4+Cu D. NaOH+HNO3=NaNO3+H2O
【题目】某兴趣小组为探究温度、压强对可逆反应A(g)+B(g) ![]() C(g)+D(s)的影响,进行了如下实验:恒温条件下,往一个容积为10 L的密闭容器中充入1 mol A和1 mol B,反应达平衡时测得容器中各物质的量浓度为[浓度1]。然后改变外界条件又做了两组实验:①只升高温度;②只改变体系压强;分别测得新平衡时容器中各物质的量浓度为[浓度2]、[浓度3]。请找出实验操作①②与实验数据[浓度2]、[浓度3]的对应关系,并分析下列结论,其中错误的是
C(g)+D(s)的影响,进行了如下实验:恒温条件下,往一个容积为10 L的密闭容器中充入1 mol A和1 mol B,反应达平衡时测得容器中各物质的量浓度为[浓度1]。然后改变外界条件又做了两组实验:①只升高温度;②只改变体系压强;分别测得新平衡时容器中各物质的量浓度为[浓度2]、[浓度3]。请找出实验操作①②与实验数据[浓度2]、[浓度3]的对应关系,并分析下列结论,其中错误的是
A | B | C | |
浓度1 | 0.05 mol·L-1 | a mol·L-1 | 0.05 mol·L-1 |
浓度2 | 0.078 mol·L-1 | 0.078 mol·L-1 | 0.022 mol·L-1 |
浓度3 | 0.06 mol·L-1 | 0.06 mol·L-1 | 0.04 mol·L-1 |
浓度4 | 0.07 mol·L-1 | 0.07 mol·L-1 | 0.098 mol·L-1 |
A. 由[浓度3]与[浓度1]的比较,可判断平衡移动的原因是增大了体系的压强
B. 由[浓度2]与[浓度1]的比较,可判断正反应是放热反应
C. [浓度1]中a=0.05
D. 该组某学生在实验①过程中,测得各物质在某一时刻的浓度为[浓度4]。与[浓度1]比较,可发现该同学在测定[浓度4]这组数据时出现了很大的误差