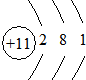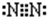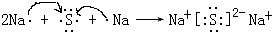题目内容
非金属单质A,经如下图所示的过程转化为含氧酸D,已知D为常见强酸

请回答下列问题:(1)若A在常温下为固体,B是能使品红溶液褪色的有刺激性气味的无色气体①D的化学式是______
②在工业生产中B气体的大量排放被雨水吸收后形成了______而污染了环境
(2)若A在常温下为气体,C是红棕色气体
①A和C的化学式分别是:A______C______
②D的浓溶液在常温下可与铜反应并生成C气体,请写出该反应的化学方程式______.
故答案为:H2SO4;
②SO2被雨水吸收后生成H2SO3和H2SO4,即形成酸雨,故答案为:酸雨;
(2)①A在常温下为气体,C是红棕色气体.据此知道含氧气体红棕色的只有NO2,故答案为:N2;NO2;
②据第一题可知D为硝酸,我们知道浓硝酸与铜反应生成NO2,故答案为:Cu+4HNO3(浓)=Cu(NO3)2+2H2O+2NO2↑.
分析:根据非金属单质可以实现上述题目转化的分别有C、S、N2,2C+O2=2CO、2CO+O2=2CO2;S+O2=S02、2SO2+O2=2SO3;N2+O2=2NO、2NO+O2=2NO2;
D为强酸,则不会是碳单质的转化;B是能使品红溶液褪色的有刺激性气味的无色气体可知B为二氧化硫,当C是红棕色气体,则C为二氧化氮,
然后依据题目可以准确做出答案.
点评:本题考查了非金属及其氧化物之间的转化;含氧酸的性质.基础性很好,对学生来说不难把握.

现有部分短周期元素的性质或原子结构如下表:
| 元素编号 | 元素性质或原子结构 |
| A | 有三个电子层,K、M层电子数之和等于L层电子数 |
| B | 短周期中金属性最强 |
| C | 常温下单质为双原子分子,氢化物的水溶液呈碱性 |
| D | 元素最高正价是+7价 |
(1)用化学用语回答下列问题:
①A元素在周期表中的位置 ;
②B元素原子结构示意图 ;
③C单质分子的电子式 ;用电子式表示A和B元素组成的化合物的形成过程 ;
④D元素在自然界有两种核素,用原子符号表示其中子数为20的核素 。
(2)元素D与元素A相比,非金属性较强的是 (用元素符号表示),下列表述中能证明这一事实的是 (填选项序号)。
a.常温下D的单质和A的单质状态不同
b.D的氢化物比A的氢化物稳定
c.一定条件下D和A的单质都能与钠反应
d.A的最高价含氧酸酸性弱于D的最高价含氧酸
e.D单质能与A的氢化物反应生成A单质
(3)探寻物质的性质差异性是学习的重要方法之一。A、B、C、D四种元素的最高价氧化物的水化物中化学性质明显不同于其他三种的是 (写化学式)。
(4)X是由A、B、C、D四种元素中的某种元素组成的单质,能经下图所示的过程转化为W(其他条件略去)。
①若Y是有刺激性气味的无色气体,把Y通入BaCl2溶液中,然后滴加适量H2O2溶液,有白色沉淀生成,此白色沉淀的化学式为: ;生成该白色沉淀的化学方程式为 ;
②若Z是红棕色气体,则Z→W的反应中氧化剂与还原剂物质的量之比为: 。
现有部分短周期元素的性质或原子结构如下表:
|
元素编号 |
元素性质或原子结构 |
|
A |
有三个电子层,K、M层电子数之和等于L层电子数 |
|
B |
短周期中金属性最强 |
|
C |
常温下单质为双原子分子,氢化物的水溶液呈碱性 |
|
D |
元素最高正价是+7价 |
(1)用化学用语回答下列问题:
①A元素在周期表中的位置 ;
②B元素原子结构示意图 ;
③C单质分子的电子式 ;用电子式表示A和B元素组成的化合物的形成过程 ;
④D元素在自然界有两种核素,用原子符号表示其中子数为20的核素 。
(2)元素D与元素A相比,非金属性较强的是 (用元素符号表示),下列表述中能证明这一事实的是 (填选项序号)。
a.常温下D的单质和A的单质状态不同
b.D的氢化物比A的氢化物稳定
c.一定条件下D和A的单质都能与钠反应
d.A的最高价含氧酸酸性弱于D的最高价含氧酸
e.D单质能与A的氢化物反应生成A单质
(3)探寻物质的性质差异性是学习的重要方法之一。A、B、C、D四种元素的最高价氧化物的水化物中化学性质明显不同于其他三种的是 (写化学式)。
(4)X是由A、B、C、D四种元素中的某种元素组成的单质,能经下图所示的过程转化为W(其他条件略去)。
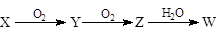
①若Y是有刺激性气味的无色气体,把Y通入BaCl2溶液中,然后滴加适量H2O2溶液,有白色沉淀生成,此白色沉淀的化学式为: ;生成该白色沉淀的化学方程式为 ;
②若Z是红棕色气体,则Z→W的反应中氧化剂与还原剂物质的量之比为: 。
现有部分短周期元素的性质或原子结构如下表:
|
元素编号 |
元素性质或原子结构 |
|
A |
有三个电子层,K、M层电子数之和等于L层电子数 |
|
B |
短周期中金属性最强 |
|
C |
常温下单质为双原子分子,氢化物的水溶液呈碱性 |
|
D |
元素最高正价是+7价 |
(1)用化学用语回答下列问题:
①A元素在周期表中的位置 ;
②B元素原子结构示意图 ;
③C单质分子的电子式 ;用电子式表示A和B元素组成的化合物的形成过程 ;
④D元素在自然界有两种核素,用原子符号表示其中子数为20的核素 。
(2)元素D与元素A相比,非金属性较强的是 (用元素符号表示),下列表述中能证明这一事实的是 (填选项序号)。
a.常温下D的单质和A的单质状态不同
b.D的氢化物比A的氢化物稳定
c.一定条件下D和A的单质都能与钠反应
d.A的最高价含氧酸酸性弱于D的最高价含氧酸
e.D单质能与A的氢化物反应生成A单质
(3)探寻物质的性质差异性是学习的重要方法之一。A、B、C、D四种元素的最高价氧化物的水化物中化学性质明显不同于其他三种的是 (写化学式)。
(4)X是由A、B、C、D四种元素中的某种元素组成的单质,能经下图所示的过程转化为W(其他条件略去)。
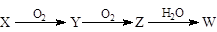
①若Y是有刺激性气味的无色气体,把Y通入BaCl2溶液中,然后滴加适量H2O2溶液,有白色沉淀生成,此白色沉淀的化学式为: ;生成该白色沉淀的化学方程式为 ;
②若Z是红棕色气体,则Z→W的反应中氧化剂与还原剂物质的量之比为: 。