题目内容
【题目】采用CO与H2反应合成再生能源甲醇,反应如下:CO(g)+ 2H2(g)![]() CH3OH(g),在一容积可变的密闭容器中充有10molCO和20mol H2,在催化剂作用下发生反应生成甲醇。CO的平衡转化率(α)与温度(T)、压强(p)的关系如图所示。则下列理解不符合题意的是
CH3OH(g),在一容积可变的密闭容器中充有10molCO和20mol H2,在催化剂作用下发生反应生成甲醇。CO的平衡转化率(α)与温度(T)、压强(p)的关系如图所示。则下列理解不符合题意的是
A. B点的速率比C点的大
B. A、B、C三点的平衡常数KA、KB、KC的大小关系为:KA=KB>KC
C. 若达到平衡状态A时,容器的体积为10L,则在平衡状态B时容器的体积为2L
D. 合成甲醇的反应为放热反应
【答案】A
【解析】A. B点到C点,升温反应速率增大,所以B点的速率比C点的小,故A不符合题意;B.升温平衡左移,K减小,所以 A、B、C三点的平衡常数KA、KB、KC的大小关系为:KA=KB>KC,故B符合题意;C. 平衡状态A时,c(CO)=0.5mol/L,c(H2)=1mol/L,c(CH3OH)=0.5mol/L,KA=![]() =1。平衡状态B时,设容器体积为xL,c(CO)=2/xmol/L,c(H2)=4/xmol/L,c(CH3OH)=8/xmol/L,KB=
=1。平衡状态B时,设容器体积为xL,c(CO)=2/xmol/L,c(H2)=4/xmol/L,c(CH3OH)=8/xmol/L,KB=![]() =KA=1,x=2,平衡状态B时容器的体积为2L,故C正确;D. 升温平衡左移,所以合成甲醇的反应为放热反应,故D正确。故选A。
=KA=1,x=2,平衡状态B时容器的体积为2L,故C正确;D. 升温平衡左移,所以合成甲醇的反应为放热反应,故D正确。故选A。

 暑假作业暑假快乐练西安出版社系列答案
暑假作业暑假快乐练西安出版社系列答案【题目】二氧化碳的回收利用是环保领域研究的热点课题。
(1)在太阳能的作用下,以CO2为原料制取炭黑的流程如右图所示,其总反应的化学方程式为_________。

(2)CO2经过催化氢化合成低碳烯烃.其合成乙烯的反应为2CO2(g)+6H2(g)![]() CH2=CH2(g)+4H2O(g)△H,已知几种化学键键能如下表所示:(CO2的结构式:O=C=O)
CH2=CH2(g)+4H2O(g)△H,已知几种化学键键能如下表所示:(CO2的结构式:O=C=O)
物质 | H-H | C=O | C=C | C-H | H-O |
能量/kJmol-1 | 436 | 745 | 615 | 413 | 463 |
则△H=_________。
(3)在2L恒容密闭容器中充入2molCO2和n molH2,在一定条件下发生(2)中的反应,CO2的转化率与温度、投料比[X= ![]() ]的关系如图所示。
]的关系如图所示。

①X1_________X2(填“>”、“<”或“=”,下同),平衡常数KA_________KB.
②若B点的投料比为3,且从反应开始到B点需要10min,则v(H2)=_______ molL-1·min-1。
(4)以稀硫酸为电解质溶液,利用太阳能将CO2转化为低碳烯烃,工作原理图如下图。(丙烯的结构简式:CH3CH=CH2)

①b电极的名称是_________;
②产生丙烯的电极反应式为_______________。
【题目】下列实验的操作、现象和解释或结论都正确的是
操作 | 现象 | 解释或结论 | |
A | 将饱和Na2SO4溶液加入到饱和石灰中 | 有白色沉淀 | 说明Ksp[Ca(OH)2]大于Ksp[CaSO4] |
B |
| 试剂瓶中有一段稳定水柱 | 装置气密性良好 |
C | 将Al2(SO4)3溶液蒸干 | 有白色固体生成 | A13+水解生成Al(OH)3 |
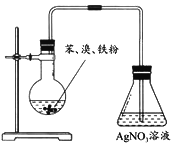
D |
| 锥形瓶溶液产生淡黄色沉淀 | 苯与溴发生取代反应 |
A. A B. B C. C D. D