题目内容
【题目】2016年9月,“乔歌里1号”中国首台静默移动发电站MFC30正式问世,MFC30是基于甲醇重整制氢燃料电池发电技术。
(1)甲醇制氢方式主要有以下三种:反应Ⅰ甲醇水蒸气重整制氢:CH3OH(g)+H2O(g) ![]() CO2(g)+3H2(g) △H1=+49.4 kJ/mol反应Ⅱ甲醇分解制氢:CH3OH(g)
CO2(g)+3H2(g) △H1=+49.4 kJ/mol反应Ⅱ甲醇分解制氢:CH3OH(g)![]() CO(g)+2H2(g) △H2=+90.6 kJ/mol反应Ⅲ气态甲醇氧化重整制氢同时生成二氧化碳和氢气:
CO(g)+2H2(g) △H2=+90.6 kJ/mol反应Ⅲ气态甲醇氧化重整制氢同时生成二氧化碳和氢气:
①已知CO的燃烧热为283.0 kJ/mol,则反应Ⅲ的热化学反应方程式为____________。
②该三种制氢方式中,等量的甲醇产生氢气最多的是反应____________。(填“Ⅰ”、“Ⅱ”、“Ⅲ”)
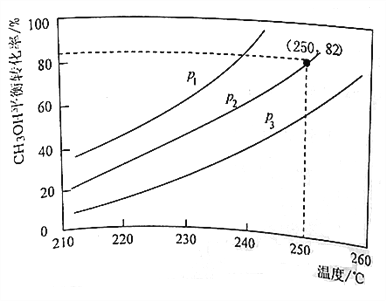
(2)实验室模拟反应Ⅰ甲醇水蒸气重整制制氢观察,合成气组成n(CH3OH): n(H2O)=1∶1时,体系中甲醇的平衡转化率与温度和压强的关系如图所示。
①该反应的平衡常数表达式为____________________。
②当温度为250℃、压强为P2时,反应达平衡时H2的体积分数为____________。
③图中的压强由小到大的顺序是____________。
(3)MFC30燃料电池是以氢为燃料,Li2CO3与K2CO3混合的碳酸盐为电解质的高温型燃料电池,其负极的电极反应式为____________,正极上通入的气体为____________。
【答案】 CH3OH(g) + 1/2O2(g) = CO2(g) + 2H2(g) △H=-192.4 kJ/mol Ⅰ K=![]()
![]() 67. 6%或0.676或0.68 P1< P2<P3 H2-2e-+CO32-=H2O+CO2 O2 (或空气),CO2
67. 6%或0.676或0.68 P1< P2<P3 H2-2e-+CO32-=H2O+CO2 O2 (或空气),CO2
【解析】 (1)已知三个反应①反应ⅠCH3OH(g)+H2O(g) ![]() CO2(g)+3H2(g) △H1=+49.4 kJ/mol,②反应ⅡCH3OH(g)
CO2(g)+3H2(g) △H1=+49.4 kJ/mol,②反应ⅡCH3OH(g)![]() CO(g)+2H2(g) △H2=+90.6 kJ/mol,③CO的燃烧热为283.0 kJ/mol,CO(g)+1/2O2(g)=CO2(g);△H=-283.0KJ·mol-1,由盖斯定律②+③得反应Ⅲ的热化学反应方程式为:CH3OH(g) + 1/2O2(g) = CO2(g) + 2H2(g) △H=-192.4 kJ/mol ;1mol甲醇产生氢气分别为3mol、2mol、2mol,最多的是反应Ⅰ。
CO(g)+2H2(g) △H2=+90.6 kJ/mol,③CO的燃烧热为283.0 kJ/mol,CO(g)+1/2O2(g)=CO2(g);△H=-283.0KJ·mol-1,由盖斯定律②+③得反应Ⅲ的热化学反应方程式为:CH3OH(g) + 1/2O2(g) = CO2(g) + 2H2(g) △H=-192.4 kJ/mol ;1mol甲醇产生氢气分别为3mol、2mol、2mol,最多的是反应Ⅰ。
(2)①反应Ⅰ甲醇水蒸气重整制氢:CH3OH(g)+H2O(g) ![]() CO2(g)+3H2(g) △H1=+49.4 kJ/mol的平衡常数为K=
CO2(g)+3H2(g) △H1=+49.4 kJ/mol的平衡常数为K= ;
;
②CH3OH(g)+H2O(g)![]() CO2(g)+3H2(g)
CO2(g)+3H2(g)
起始 /mol 1 1 0 0
反应 /mol 0.82 0.82 0.82 3×0.82
平衡 /mol 0.18 0.18 0.82 2.46
反应达平衡时H2的体积分数为
2.46/[0.18+0.18+0.82+2.46]=0.676
③由方程式CH3OH(g)+H2O(g) ![]() CO2(g)+3H2(g),相同温度时,减小压强,平衡正向移动,CH3OH转化率增大,由图从P3到P1压强减小,图中的压强由小到大的顺序是P1< P2<P3。
CO2(g)+3H2(g),相同温度时,减小压强,平衡正向移动,CH3OH转化率增大,由图从P3到P1压强减小,图中的压强由小到大的顺序是P1< P2<P3。
(3)燃料电池中通入燃料的电极是负极、通入氧化剂的电极是正极,负极是H2作还原剂,H2-2e-+CO32-=H2O+CO2 ,正极上氧气得电子和二氧化碳反应生成碳酸根离子,电极反应式为O2+2CO2-4e-═2CO32-,故正极要不断通入O2 (或空气),CO2。