题目内容
关于常温下pH=2的醋酸溶液,下列叙述正确的是
| A.c(CH3COOH)=0.01mol·L-1 |
| B.c(H+)=c(CH3COO-) |
| C.加水稀释100倍后,溶液pH=4 |
| D.醋酸的电离常数为Ka,CH3COO-的水解常数为Kh,则Ka·Kh=Kw |
D
醋酸部分电离,它的起始物质的量浓度比c(H+)大得多,A错;由于水也电离出H+,c(H+)>c(CH3COO-)B错;加水稀释100倍,pH上升不到2个单位,C错。Kh=c(OH-)(CH3COOH)/c(CH3COO-),给表达式上下同乘以c(H+),方可推断出Ka·Kh=Kw。答案选D。

练习册系列答案
相关题目
 I—+ I2。实验室可以通过氧化还原滴定法测定平衡时I3—的浓度
I—+ I2。实验室可以通过氧化还原滴定法测定平衡时I3—的浓度 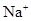 )>c(
)>c(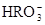 )>c(
)>c(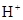 )>c(
)>c(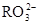 )>c(
)>c(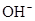 )
)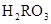 )=c(
)=c(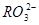 )分别相等
)分别相等