题目内容
【题目】NH4Al(SO4)2是食品加工中最为快捷的食品添加剂,用于焙烤食品;NH4HSO4在分析试剂、医药、电子工业中用途广泛。请回答下列问题:
(1)相同条件下,0.1 mol·L-1NH4Al(SO4)2溶液中c((NH4+)_________(填“等于”、“大于”或“小于”) 0.1 mol·L-1NH4HSO4溶液中c(NH4+)
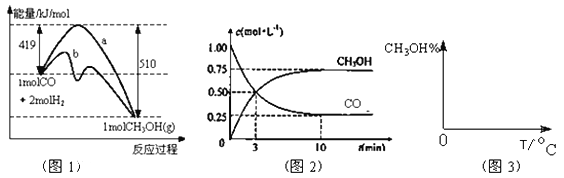
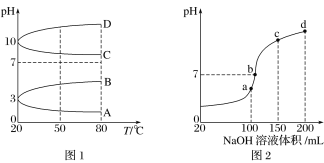
(2)如图1是0.1 mol·L-1电解质溶液的pH随温度变化的图像。
①其中符合0.1 mol·L-1NH4Al(SO4)2溶液的pH随温度变化的曲线是______(填字母)。
②室温时,0.1 mol·L-1NH4Al(SO4)2溶液中2c(SO42-)- c(NH4+)-3c(Al3+)=________ mol·L-1
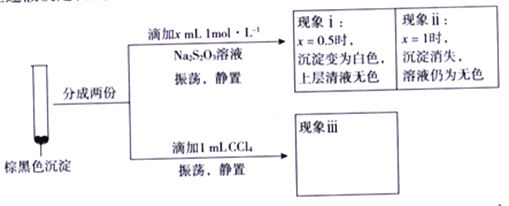
(3)室温时,向100 mL 0.1 mol·L-1NH4HSO4溶液中滴加0.1 mol·L-1NaOH溶液,得到的溶液pH与NaOH溶液体积的关系曲线如图2所示。 试分析图中a、b、c、d四个点,水的电离程度最大的是____________; 在b点,溶液中各离子浓度由大到小的排列顺序是___________________。
(4)用0.1mol/LNaOH溶液滴定盐酸溶液,下列操作中使结果偏高的是___________________
A.盛标准溶液的滴定管用蒸馏水洗涤后未用标准液润洗就装液滴定
B.锥形瓶用蒸馏水洗涤后未用待测液润洗
C.读取标准液读数时,滴定前平视,滴定到终点后俯视
D.滴定前盛标准液的滴定管尖嘴处有气泡未排除,滴定后气泡消失
【答案】小于 A 10-3(或10-3-10-11) a c(Na+)>c(SO42-)>c(NH4+)>c(OH-)=c(H+) AD
【解析】
(1)NH4Al(SO4)2中Al3+水解使溶液显酸性,可抑制NH4+的水解,HSO4-电离出H+,也能抑制NH4+的水解;
(2)①NH4Al(SO4)2水解使溶液显酸性,升高温度其水解程度增大;
②根据电荷守恒分析解答;
(3)a、b、c、d4个点,a点恰好将H+消耗完,溶液中只有(NH4)2SO4与Na2SO4,b、c、d三点溶液均含有NH3H2O,(NH4)2SO4可以促进水的电离,而NH3H2O抑制水的电离,b点溶液呈中性;
(4)根据c(待测)= 判断不当操作度相关物理量的影响。
判断不当操作度相关物理量的影响。
(1)NH4Al(SO4)2与NH4HSO4中的NH4+均发生水解,但NH4Al(SO4)2中Al3+水解使溶液显酸性,可抑制NH4+的水解,HSO4-电离出H+,也能抑制NH4+的水解,因HSO4-电离出的H+浓度大于Al3+水解生成的H+浓度,因此NH4HSO4溶液中c((NH4+)小于0.1 mol·L-1NH4HSO4溶液中c(NH4+);
(2)①NH4Al(SO4)2水解使溶液显酸性,升高温度其水解程度增大,pH减小,符合的曲线为A;
②根据电荷守恒,可以得出2c(SO42-)-c(NH4+)-3c(Al3+)=c(H+)-c(OH-)=10-3mol/L-10-11mol/L≈10-3mol/L;
(3)a、b、c、d4个点,a点恰好将H+消耗完,溶液中只有(NH4)2SO4与Na2SO4,b、c、d三点溶液均含有NH3H2O,(NH4)2SO4可以促进水的电离,而NH3H2O抑制水的电离,b点溶液呈中性,即溶液中含有NH3H2O、(NH4)2SO4、Na2SO4三种成分,a点c(Na+)=c(SO42-),b点c(Na+)>c(SO42-),根据N元素与S元素的关系,可以得出c(SO42-)>c(NH4+),因此有:c(Na+)>c(SO42-)>c(NH4+)>c(OH-)=c(H+);
(4)A. 盛标准溶液的滴定管用蒸馏水洗涤后未用标准液润洗就装液滴定,标准液浓度减小,所需标准液的体积增大,导致待测液的浓度偏高,A项正确;
B. 锥形瓶用蒸馏水洗涤后未用待测液润洗,所需的标准液的体积不变,导致待测液的浓度不变,B项错误;
C. 读取标准液读数时,滴定前平视,滴定到终点后俯视,所需标准液的体积偏小,导致待测液的浓度偏小,C项错误;
D. 滴定前盛标准液的滴定管尖嘴处有气泡未排除,滴定后气泡消失,所需标准液的体积偏大,导致待测液的浓度偏大,D项正确;
答案选AD。

 阅读快车系列答案
阅读快车系列答案【题目】在25℃时,密闭容器中X、Y、Z三种气体的初始浓度和平衡浓度如下表:
物质 | X | Y | Z |
初始浓度/mol·L1 | 0.1 | 0.2 | 0 |
平衡浓度/mol·L1 | 0.05 | 0.05 | 0.1 |
下列说法错误的是( )
A.反应达到平衡时,X的转化率为50%
B.反应可表示为X+3Y![]() 2Z,其平衡常数为1600
2Z,其平衡常数为1600
C.增大压强使平衡向生成Z的方向移动,平衡常数增大
D.改变温度可以改变此反应的平衡常数