题目内容
天然存在的金属钫(Fr)极微量.它的21种已知同位素都有放射性.它是碱金属元 素中最重的元素.根据它在周期表中的位置预言其性质,其中不正确的是( )
| A、在空气中燃烧时生成氧化物Fr2O |
| B、在已知元素中具有最大的原子半径 |
| C、氧化物对应的水化物碱性极强 |
| D、其单质的熔点比金属钠的熔点低 |
考点:碱金属的性质
专题:元素周期律与元素周期表专题,金属概论与碱元素
分析:A.依据同主族元素金属性从上到下依次递增解答;
B.依据钫在周期表中第七周期,ⅠA族的位置,结合同周期、同主族元素原子半径的规律解答;
C.元素金属性越强,氧化物对应水化物的碱性越强;
D.依据同主族金属元素熔点从上到下依次的降低的规律解答.
B.依据钫在周期表中第七周期,ⅠA族的位置,结合同周期、同主族元素原子半径的规律解答;
C.元素金属性越强,氧化物对应水化物的碱性越强;
D.依据同主族金属元素熔点从上到下依次的降低的规律解答.
解答:
解:A.钫与钠、钾同主族,位于钠和钾的下方,所以活泼性强于钠和钾,钠在空气中燃烧生成过氧化钠,钾在空气中燃烧生成超氧化钾,所以钫在空气中燃烧时生成氧化物FrO2,故A错误;
B.同主族元素原子半径从上到下依次增大,同周期元素原子半径从左到右依次减小,钫位于周期表中最左下方,所以原子半径最大,故B正确;
C.同主族元素金属性从上到下依次增强,钫位于第ⅠA族的最下方,所以其金属性最强,所以氧化物对应的水化物碱性极强,故C正确;
D.同主族金属元素熔点从上到下依次的降低,故D正确;
故选:A.
B.同主族元素原子半径从上到下依次增大,同周期元素原子半径从左到右依次减小,钫位于周期表中最左下方,所以原子半径最大,故B正确;
C.同主族元素金属性从上到下依次增强,钫位于第ⅠA族的最下方,所以其金属性最强,所以氧化物对应的水化物碱性极强,故C正确;
D.同主族金属元素熔点从上到下依次的降低,故D正确;
故选:A.
点评:本题考查了钫的性质,明确元素性质的递变规律是解题关键,注意元素金属性强弱的判断依据.

练习册系列答案
相关题目
在乙醇发生的各种反应中,断键方式不正确的是( )
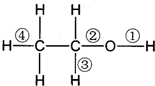

| A、与金属钠反应时,键①断裂 |
| B、与醋酸、浓硫酸共热时,键②断裂 |
| C、与浓硫酸共热至170℃时,键②和④断裂 |
| D、与HCl反应生成氯乙烷时,键②断裂 |
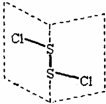 二氯化二硫(S2Cl2)是广泛用于橡胶工业的硫化剂,其分子结构如图所示,遇水易水解,并产生能使品红褪色的气体.S2Br2与S2Cl2结构相似.下列说法错误的是( )
二氯化二硫(S2Cl2)是广泛用于橡胶工业的硫化剂,其分子结构如图所示,遇水易水解,并产生能使品红褪色的气体.S2Br2与S2Cl2结构相似.下列说法错误的是( )| A、S2Cl2中硫原子轨道杂化类型为sp3杂化 |
| B、S2Cl2为含有极性键和非极性键的非极性分子 |
| C、熔沸点:S2Br2>S2Cl2 |
| D、S2Cl2与H2O反应的化学方程式可能为:2S2Cl2+2H2O═SO2↑+3S↓+4HCl |
美国亚利桑那州大学(ASU)和阿贡国家实验室的科学家最近设计出生产氢气的人造树叶,原理为:2H2O(g)
2H2(g)+O2(g).有关该反应的说法正确的是( )
| ||
| 人造树叶 |
| A、△H<0 |
| B、△S<0 |
| C、化学能转变为电能 |
| D、氢能是理想的绿色能源 |
取100mL 0.3mol/L和300mL 0.25mol/L的硫酸注入500mL容量瓶中,加水稀释至刻度线,该混合溶液中H+的物质的量浓度是( )mol/L.
| A、0.21 | B、0.42 |
| C、0.56 | D、0.26 |
设NA表示阿伏伽德罗常数的值,下列说法中正确的( )
| A、常温下,42g C2H4和C4H8的混合物中含有的碳原子数为3NA |
| B、58.5g氯化钠固体中含有NA个氯化钠分子 |
| C、标况下,11.2L己烷所含的分子数为0.5NA |
| D、1mol FeCl3完全水解转化为氢氧化铁胶体后生成NA个胶粒 |
下列各组物质中,互为同分异构体的是( )
| A、O2与O3 | ||||
B、
| ||||
| C、CH2Cl2与CHCl3 | ||||
D、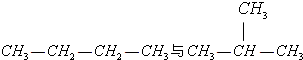 |