题目内容
【题目】某密闭容器中发生反应:X(g) + 3Y(g)![]() 2Z(g) ΔH < 0。图表示该反应的速率(v)随时间(t)变化的关系,t2、t3、t5时刻外界条件有所变化,但都没有改变各物质的初始加入量。下列说法正确的是( )
2Z(g) ΔH < 0。图表示该反应的速率(v)随时间(t)变化的关系,t2、t3、t5时刻外界条件有所变化,但都没有改变各物质的初始加入量。下列说法正确的是( )
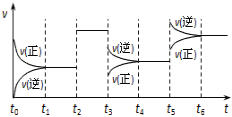
A.t2时加入了催化剂B.t3时降低了温度
C.t5时增大了压强D.t4~t5时间内反应物转化率最低
【答案】A
【解析】
A、t2时正逆反应速率增大相同的倍数,平衡不移动。由于反应前后体积是减小的,所以改变的条件只能是加入了催化剂,选项A正确;
B、正反应是放热反应,降低温度,平衡向正反应方向进行,正反应速率大于逆反应速率,选项B不正确;
C、增大压强,平衡向正反应方向进行,正反应速率大于逆反应速率,选项C不正确;
D、t3和t5都是平衡逆向移动,故应该是t6时转化率最低,选项D不正确;
答案选A。

练习册系列答案
 优加精卷系列答案
优加精卷系列答案
相关题目
【题目】Na、Cu、O、Si、S、Cl是常见的六种元素。
(1)Na位于元素周期表第____周期第____族;S的基态原子核外有________个未成对电子;Si的基态原子核外电子排布式为__________。
(2)用“>”或“<”填空:
第一电离能 | 离子半径 | 熔点 | 酸性 |
Si____S | O2-____Na+ | NaCl____Si | H2SO4____HClO4 |
【题目】现有A、B、C、D、E五种均可溶于水的固体物质,是由以下提供的几种离子组成![]() 每种离子只能用一次
每种离子只能用一次![]() :
:
阳离子 |
|
阴离子 |
|
现分别进行如下实验:
![]() 将D与E的溶液混合加热,产生有刺激性气味的气体
将D与E的溶液混合加热,产生有刺激性气味的气体
![]() 将B与E的溶液混合,产生白色沉淀,向该沉淀中加入足量的稀硝酸,沉淀部分溶解
将B与E的溶液混合,产生白色沉淀,向该沉淀中加入足量的稀硝酸,沉淀部分溶解
![]() 在常温下用pH试纸测定溶液A的
在常温下用pH试纸测定溶液A的![]()
下列说法不正确的是![]()
A.物质E的化学式为![]() B.物质D中一定含有
B.物质D中一定含有![]()
C.难以确定物质A的组成D.物质C的化学式是![]()