题目内容
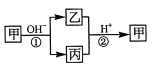
【题目】I.A、B、C、D四种均为含有钠元素的化合物,A、B、C与盐酸反应均可生成D;加热固体C可生成A和一种无色无味的气体X;在A溶液中通入足量X,又可生成C;B溶液和C溶液混合可生成A。请回答:
(1)B是___________,D是___________,(均用化学式表示)
(2)写出上述反应中由A生成C的化学方程式:____________________________________。
II.化合物甲仅含两种元素。B为黄绿色气体,气体D能使湿润的红色石蕊试纸变蓝色。在一定条件下有如下转化关系:
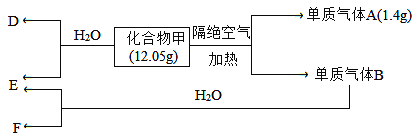
请回答:
(1)化合物甲所含元素为__________(填写元素符号),甲的化学式为___________________。
(2)气体B与水反应的离子方程式为____________________________________。
(3)甲与水反应的化学方程式为____________________________________。
【答案】NaOH NaCl Na2CO3+CO2+H2O=2NaHCO3 N、Cl NCl3 Cl2+H2O![]() H++Cl-+HClO NCl3+3H2O=NH3+3HClO
H++Cl-+HClO NCl3+3H2O=NH3+3HClO
【解析】
I.A、B、C、D四种均为含有钠元素的化合物,A、B、C分别和足量的盐酸反应后,均可生成D,则D为NaCl,将固体C加热后可生成A和无色无味的气体X,则C为NaHCO3、A为Na2CO3、E为CO2,在Na2CO3溶液中通入足量CO2可生成NaHCO3,B与NaHCO3的溶液混合可生成Na2CO3,则B为NaOH。
II.B 为黄绿色气体,B为Cl2,气体D能使湿润的红色石蕊试纸变蓝色,D为NH3,结合图中转化可知,甲含N、Cl元素,且B与水反应生成HCl、HClO,甲与水反应生成D、E,则E为HClO,F为HCl,12.05g甲含N元素为1.4g,A为N2,甲中N、Cl原子个数比为![]() =1:3,可知甲的化学式为NCl3。
=1:3,可知甲的化学式为NCl3。
I.A、B、C、D四种均为含有钠元素的化合物,A、B、C分别和足量的盐酸反应后,均可生成D,则D为NaCl,将固体C加热后可生成A和无色无味的气体X,则C为NaHCO3、A为Na2CO3、E为CO2,在Na2CO3溶液中通入足量CO2可生成NaHCO3,B与NaHCO3的溶液混合可生成Na2CO3,则B为NaOH。
(1)B 是 NaOH,D 是 NaCl;
(2)上述反应中由A生成C的化学方程式:Na2CO3+CO2+H2O=2NaHCO3;
II.B 为黄绿色气体,B为Cl2,气体D能使湿润的红色石蕊试纸变蓝色,D为NH3,结合图中转化可知,甲含N、Cl元素,且B与水反应生成HCl、HClO,甲与水反应生成D、E,则E为HClO,F为HCl,12.05g甲含N元素为1.4g,A为N2,甲中N、Cl原子个数比为![]() =1:3,可知甲的化学式为NCl3。
=1:3,可知甲的化学式为NCl3。
(1)由元素守恒可知化合物甲所含元素为N、Cl,甲的化学式为NCl3。
(2)气体B 与水反应的离子方程式为Cl2+H2O![]() H++Cl-+HClO;
H++Cl-+HClO;
(3)甲与水反应的化学方程式为NCl3+3H2O=NH3+3HClO。