��Ŀ����
����Ŀ��ij�ȵ糧������õ���ʯ�ࣨCaSO42H2O������K2SO4���ϵ�������ͼ��
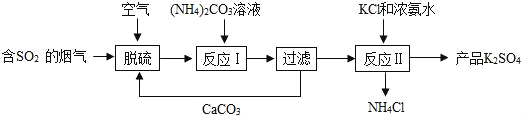
��ش��������⣺
��1��ʯ����S�Ļ��ϼ���___���Ի���S2-�����ӽṹʾ��ͼ___����д��������̵Ļ�ѧ����ʽ2CaCO3+2SO2+O2+4H2O��2CaSO42H2O+2__��
��2��ʯ���뱥�ͣ�NH4��2CO3��Һ���ϣ�������Ӧ��ʱ�費�Ͻ��裬��Ŀ����__��
��3��ʵ������ɹ��˲�������Ҫ�õ�����������������������____��
��4���ù��տ���ѭ�����õ�������____������ƷNH4Clũҵ�����п�����___��
���𰸡�+6  CO2 ʹԭ�ϳ�ַ�Ӧ�����ԭ�������� ���� ̼��� ����
CO2 ʹԭ�ϳ�ַ�Ӧ�����ԭ�������� ���� ̼��� ����
��������
(1)�����������ϼ۵Ĵ�����Ϊ0����S�Ļ��ϼۣ�S2-�ĺ˵����Ϊ16�����⺬��18�����ӣ���Ϻ�����ӵ��Ų����ɻ������ӽṹʾ��ͼ�����������غ㶨�ɷ����жϣ�
(2)���ݽ����ܹ�ʹԭ�ϳɷֻ�Ϸ�����
(3)���ݹ��˲����в����������÷�����
(4)���ݷ�Ӧ�����еķ�Ӧ�������ҳ���ѭ�����õ����ʣ�����NH4Cl����NԪ�ط�����
(1)ʯ��(CaSO42H2O)��Ca�Ļ��ϼ�Ϊ+2�ۣ�H�Ļ��ϼ�Ϊ+1�ۣ�O�Ļ��ϼ�Ϊ-2�ۣ������������ϼ۵Ĵ�����Ϊ0��S�Ļ��ϼ���+6�ۣ�S2-�ĺ˵����Ϊ16�����⺬��18�����ӣ����ӽṹʾ��ͼΪ ���������غ㶨�ɣ���Ӧǰ��ԭ�ӵ����༰��Ŀ�����֪��������������Ӧ����������ǣ�CO2���ʴ�Ϊ��+6��
���������غ㶨�ɣ���Ӧǰ��ԭ�ӵ����༰��Ŀ�����֪��������������Ӧ����������ǣ�CO2���ʴ�Ϊ��+6�� ��CO2��
��CO2��
(2)ʯ���뱥��(NH4)2CO3��Һ���ϣ�������Ӧ��ʱ�費�Ͻ��裬����ʹԭ�ϳ�ַ�Ӧ�����ԭ�������ʣ��ʴ�Ϊ��ʹԭ�ϳ�ַ�Ӧ�����ԭ�������ʣ�
(3)ʵ������ɹ��˲�����Ҫ�ò�������������ֹҺ������©���⣬�ʴ�Ϊ��������
(4)ͨ��������Ӧ�����̿�֪���ù��տ���ѭ�����õ�������̼��ƣ�NH4Cl�dz�����һ�ֵ��ʣ��ʴ�Ϊ��̼��ƣ����ʡ�

 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
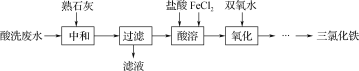
Сѧ��10����Ӧ����ϵ�д�����Ŀ�������ӹ�ǰ��������Խ������������������ϴ���������ϴ��ˮ��pH��2���ҵ�ij���Է�ˮ����Ԫ����������Լ3%����������Ԫ����ͭ������пŨ�Ƚϵͣ��ۺ�������ϴ��ˮ���Ʊ����Ȼ������Ʊ��������£�
��ؽ������������������������pH���±���
Fe(OH)3 | Cu(OH)2 | Ni(OH)2 | Zn(OH)2 | |
��ʼ������pH | 1.5 | 4.2 | 7.1 | 5.4 |
������ȫ��pH | 3.7 | 6.7 | 9.2 | 8.0 |
�ش��������⣺
(1)���к͡�ʱ����pH��________�������ں����Ʊ��ô��ȽϸߵIJ�Ʒ��
(2)������ϴ��ˮ�кͺ��������ʹ��Ԫ�ؽ��������ղ�ͬ�Ĺ�Һ��Ͷ�롰���ˡ���������ҵ������з�Ӧ������������ͼ��ʾ��ʵ�������й�Һ��ѡ��1.5��1��ԭ����__________________��
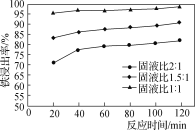
(3)д�����������з�����Ӧ�����ӷ���ʽ��____________________________________��
(4)�����ܡ����������Һ��Fe2������ȷ����������Ͷ��������K2Cr2O7����Һ�ⶨFe2��(Cr2O![]() ����ԭΪCr3��)�ĺ������÷�Ӧ���ӷ���ʽΪ____________________________��
����ԭΪCr3��)�ĺ������÷�Ӧ���ӷ���ʽΪ____________________________��
(5) �����Ȼ�����Һ��һ��������________��________�����ˡ�ϴ�ӡ����Ȼ��������и����FeCl3��6H2O���壬��ʵ���ҹ���װ����ϴ�ӹ���ķ�����___________________��