题目内容
【题目】在2 L的密闭容器中有如图所示的反应,看图按要求回答下列问题:
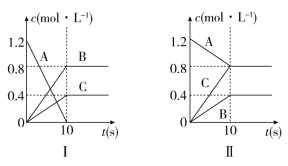
(1)图Ⅰ中反应物是________,Ⅱ中反应物是________。
(2)写出反应方程式:
Ⅰ_____________________________,
Ⅱ_____________________________。
(3)在图Ⅱ中,以0~10 s内的平均反应速率计算,t=6 s时A的浓度是________mol·L-1。
【答案】(1)A;A (2)3A=2B+C;A![]() B+2C (3)0.96mol/L
B+2C (3)0.96mol/L
【解析】
试题分析:(1)图Ⅰ、Ⅱ分析图象变化可知,都是A的浓度随反应进行不断减小至不变,B、C浓度随反应进行而不断增加至不变化,所以A为反应物,B、C为生成物;
(2)上述分析和图像变化可知,Ⅰ反应中,10s末,A浓度变化为1.2 mol/L,B、C的浓度从0变化为0.8 mol/L,0.4 mol/L,说明该反应不是可逆反应,c(A):c(B):c(C) = 1.2:0.8:0.4 = 3:2:1,反应的化学方程式为:3A=2B+C;Ⅱ反应中,10s末,A浓度变化为1.2 mol/L-0.8 mol/L = 0.4 mol/L,B、C的浓度从0变化为0.4 mol/L,0.8 mol/L,说明该反应是可逆反应,c(A):c(B):c(C) = 0.4:0.4:0.8 = 1:1:2,反应的化学方程式为:A![]() B+2C;
B+2C;
(3)在Ⅱ图中图像分析可知反应的速率匀速进行,计算10s时A的反应速率V(A) = 0.4 mol/L÷10s = 0.04 mol/(Ls),6s时变化的A的浓度c(A) = 6s × V(A) = 0.04 mol/(Ls) × 6s = 0.24 mol/L,最后得到A的浓度 = 1.2 mol/L-变化的A的浓度c(A) = 1.2 mol/L-0.24 mol/L = 0.96 mol/L。

 新课标快乐提优暑假作业陕西旅游出版社系列答案
新课标快乐提优暑假作业陕西旅游出版社系列答案