题目内容
下列物质的变质过程中,既有氧化还原反应,又有非氧化还原反应的是( )
| A.Ca(ClO)2 | B.NaOH | C.FeSO4 | D.Na2SO3 |
A
试题分析:Ca(ClO)2在空气中变质,先发生Ca(ClO)2+CO2+H2O=CaCO3+2HClO,然后再发生2HClO
 2HCl +O2↑,因此既有非氧化还原反应,又有氧化还原反应。NaOH在空气中变质生成Na2CO3,属于非氧化还原反应。FeSO4在空气中变质生成Fe2(SO4)3,属于氧化还原反应。Na2SO3在空气中变质生成Na2SO4,属于氧化还原反应。答案选A。
2HCl +O2↑,因此既有非氧化还原反应,又有氧化还原反应。NaOH在空气中变质生成Na2CO3,属于非氧化还原反应。FeSO4在空气中变质生成Fe2(SO4)3,属于氧化还原反应。Na2SO3在空气中变质生成Na2SO4,属于氧化还原反应。答案选A。点评:是不是氧化还原反应只要看反应中是否有元素的化合价发生改变。

练习册系列答案
相关题目
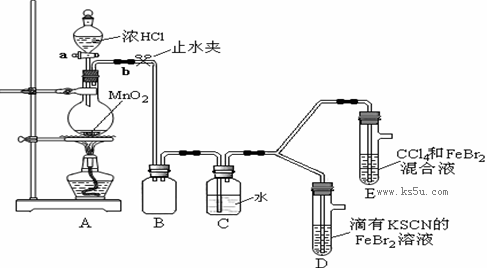

 (1)2FeCl3+2KI===2FeCl2+l2+2KCI; (2)2FeCl2+C12=2FeCl3
(1)2FeCl3+2KI===2FeCl2+l2+2KCI; (2)2FeCl2+C12=2FeCl3