题目内容
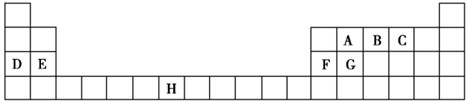
下图是元素周期表的一部分,表中的①~⑩中元素,用元素符号或化学式填空回答:
|
周期 |
ⅠA |
ⅡA |
ⅢA |
ⅣA |
ⅤA |
ⅥA |
ⅦA |
0 |
|
二 |
|
|
|
|
① |
|
② |
|
|
三 |
③ |
④ |
⑤ |
⑥ |
|
|
⑦ |
⑧ |
|
四 |
⑨ |
|
|
|
|
|
⑩ |
|
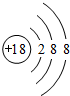
⑴在这些元素中,化学性质最不活泼元素的原子结构示意图为 。
⑵得电子能力最强的是 地壳中含量最多的金属元素是 。
⑶用电子式表示②与④形成化合物的过程 。
⑷这些元素中的最高价氧化物对应的水化物中,酸性最强的是 ,碱性最强的是 ,呈两性的氢氧化物是 。
⑸比较②③④⑦形成的简单离子半径的大小 。
⑹某元素R的气态氢化物为HXR,且R在该氢化物中的质量分数为94%,8.5g的HXR气体在标准状态下的体积是5.6L。则HXR的相对分子量为 ;HXR的化学式为 。
(每空1分,共10分)
(1)Ar结构示意图略 (2)F Al (3) (4)HClO4 KOH Al(OH)3
(4)HClO4 KOH Al(OH)3
(5)Cl-〉 F- 〉Na+ 〉Mg2+ (6) 34 H2S
【解析】
试题分析:由元素在周期表中的位置可知,①为N,②为F,③为Na,④为Mg,⑤为Al,⑥为Si,⑦为Cl,⑧为Ar,⑨为K,⑩为Br,
(1)以上元素中只有Ar的最外层电子数为8,性质不活泼,最稳定,其原子结构示意图为 ;
;
(2)得电子能力最强的是F,地壳中元素的含量较多的有O、Si、Al、Ca,则金属元素最多的为Al。
(3)②与④形成的化合物为MgF2,为离子化合物,其电子式为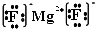 ,所以MgF2的形成过程是
,所以MgF2的形成过程是 ;
;
(4)以上元素中最高价氧化物对应的水化物中酸性最强的为HClO4,碱性最强的为KOH,呈两性的氢氧化物为Al(OH)3,故答案为:HClO4;KOH;Al(OH)3;
(5)②③④⑦形成的简单离子半径的大小为Cl-〉 F- 〉Na+ 〉Mg2+。
⑹HxR气体在标准状况下的体积是5.6L,说明物质的量为5.6/22.4=0.25mol,又因为气体质量为8.5g,所以摩尔质量为8.5/0.25=34因此HxR的相对分子质量为34,R在该氢化物中的质量分数为94%,所以R的原子量为34*0.94=31.96=32,所以R是硫,因此HxR的化学式为H2S。
考点:元素周期律和元素周期表的综合应用
点评:本题考查元素周期表和元素周期律,熟悉元素在周期表中的位置是解答本题的关键,难度不大,注意化学用语的使用来解答。

 族
族