题目内容
11.下列判断或叙述正确的是( )| A. | 某无色溶液中加入AgNO3溶液得白色沉淀,加稀硝酸沉淀不消失,则原溶液一定存在Cl-或CO32- | |
| B. | 某无色溶液中滴加BaCl2溶液得白色沉淀,加稀硝酸沉淀不溶解,则一定含有SO42- | |
| C. | 做水的蒸馏实验时,要在烧瓶内加几粒沸石以防止暴沸 | |
| D. | 某无色溶液中滴加CaCl2溶液得白色沉淀,若加入盐酸则生成无色气体,该气体能使澄清石灰水变浑浊,则原溶液中一定有CO32- |
分析 A.碳酸银能够溶于稀硝酸,原溶液中一定不含碳酸根离子;
B.该沉淀可能为氯化银,原溶液中可能含有银离子;
C.液体混合物在加热时易爆沸,可加入沸石防止爆沸;
D.原溶液中可能含有碳酸氢根离子.
解答 解:A.某无色溶液中加入AgNO3溶液得白色沉淀,加稀硝酸沉淀不消失,该沉淀为AgCl,则原溶液一定存在Cl-,一定不含CO32-,故A错误;
B.某无色溶液中滴加BaCl2溶液得白色沉淀,加稀硝酸沉淀不溶解,生成的沉淀可能为硫酸钡或AgCl,原溶液中可能含有氯离子.不一定含有SO42-,故B错误;
C.做水的蒸馏实验时,为了防止爆沸,需要在烧瓶内加几粒沸石,故C正确;
D.无色溶液中滴加CaCl2溶液得白色沉淀,若加入盐酸则生成无色气体,该气体能使澄清石灰水变浑浊,该气体可能为二氧化碳或二氧化硫,则原溶液中可能含有碳酸氢根离子、亚硫酸根离子等,不一定有CO32-,故D错误;
故选C.
点评 本题考查了常见离子的检验方法,题目难度中等,明确常见离子的性质为解答关键,注意熟练掌握常见离子的检验方法,试题培养了学生的分析能力及灵活运用能力.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
1.原央视记者柴静自费拍摄了雾霾纪录片《穹顶之下》,提醒人们必须十分重视环境问题.以下有关说法正确的是( )
| A. | 实验结束后将所有的废液倒入下水道排出实验室,以免污染实验室 | |
| B. | 为了使养分还田而将植物秸秆焚烧处理 | |
| C. | PM2.5是指大气中直径接近于2.5×10-6m(1m=109nm)的颗粒物,这些细颗粒物分散在空气中形成的分散系是胶体 | |
| D. | 实现资源的“3R”利用,即:减少资源消耗(Reduce)、增加资源的重复使用(Reuse)、提高资源的循环利用(Recycle) |
2. 已知:CO(g)+H2O(g)?CO2(g)+H2(g)△H=Q,其平衡常数随温度变化如下表所示:
已知:CO(g)+H2O(g)?CO2(g)+H2(g)△H=Q,其平衡常数随温度变化如下表所示:
请回答下列问题:
(1)上述反应的化学平衡常数表达式为$\frac{c(C{O}_{2})×c({H}_{2})}{c(CO)×c({H}_{2}O)}$.该反应的Q<0(填“>”或“<”).
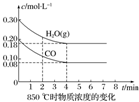
(2)850℃时在体积为10L的反应器中,通入一定量的CO和H2O(g),发生上述反应,CO和H2O(g)的物质的量浓度变化如图所示,则0~4min时平均反应速率v(CO)=0.03mol/(L•min).
(3)若在500℃时进行.且CO、H2O(g)的起始浓度均为0.020mol•L-1,该条件下,CO的最大转化率为75%.
(4)若在850℃时进行,设起始时CO和H2O(g)共为1mol,其中H2O(g)的体积分数为x,平衡时CO的转化率为y,试推导y与x之间的关系x=y.
 已知:CO(g)+H2O(g)?CO2(g)+H2(g)△H=Q,其平衡常数随温度变化如下表所示:
已知:CO(g)+H2O(g)?CO2(g)+H2(g)△H=Q,其平衡常数随温度变化如下表所示:| 温度/℃ | 400 | 500 | 850 |
| 平衡常数 | 9.94 | 9 | 1 |
(1)上述反应的化学平衡常数表达式为$\frac{c(C{O}_{2})×c({H}_{2})}{c(CO)×c({H}_{2}O)}$.该反应的Q<0(填“>”或“<”).
(2)850℃时在体积为10L的反应器中,通入一定量的CO和H2O(g),发生上述反应,CO和H2O(g)的物质的量浓度变化如图所示,则0~4min时平均反应速率v(CO)=0.03mol/(L•min).
(3)若在500℃时进行.且CO、H2O(g)的起始浓度均为0.020mol•L-1,该条件下,CO的最大转化率为75%.
(4)若在850℃时进行,设起始时CO和H2O(g)共为1mol,其中H2O(g)的体积分数为x,平衡时CO的转化率为y,试推导y与x之间的关系x=y.
19.硫有多种单质.S(单斜)和S(正交)是其中的两种同素异形体.已知:
①S(单斜,s)+O2(g)═SO2(g)△H1=-297.16kJ•mol-1
②S(正交,s)+O2(g)═SO2(g)△H2=-296.83kJ•mol-1
③S(单斜,s)═S(正交,s)△H3
下列说法不正确的是( )
①S(单斜,s)+O2(g)═SO2(g)△H1=-297.16kJ•mol-1
②S(正交,s)+O2(g)═SO2(g)△H2=-296.83kJ•mol-1
③S(单斜,s)═S(正交,s)△H3
下列说法不正确的是( )
| A. | △H3<0 | |
| B. | 正交硫比单斜硫稳定 | |
| C. | 单斜硫转化为正交硫是吸热反应 | |
| D. | 质量相等时,单斜硫能量比正交硫能量高 |
6.下列有关物质的分类正确的是( )
| A. | 混合物:空气、矿泉水、水银 | B. | 酸性氧化物:、CO2、SO2、CO | ||
| C. | 盐:醋酸钠、氯化铵、纯碱 | D. | 弱电解质:CH3COOH、H2O、NH3 |
16.CO2、H2和CO组成的混合气体在同温同压下与氮气的密度相同.则该混合气体中CO2、H2和CO的体积比不可能的为( )
| A. | 13:8:29 | B. | 39:24:13 | C. | 22:11:14 | D. | 26:16:57 |
20.某溶液X中可能含有NO3-、Cl-、SO42-、CO32-、NH4+、Fe2+、Fe3+、Al3+和K+中的几种,且所含阴离子的物质的量相等.为确定该溶液X的成分,某学习小组做了如图实验,则下列说法正确的是( )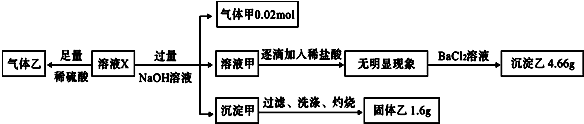

| A. | 气体甲、沉淀甲一定为纯净物 | |
| B. | CO32-、Al3+、K+一定不存在 | |
| C. | SO42-、NH4+一定存在,NO3-、Cl-可能不存在 | |
| D. | 若含有Fe3+,则一定含有Cl- |
7.相同温度下,在体积相等的三个恒容密闭容器中发生可逆反应:
N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ/mol
实验测得起始、平衡时的有关数据如下表:
下列叙述正确的是( )
N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ/mol
实验测得起始、平衡时的有关数据如下表:
| 容器编号 | 起始时各物质物质的量/mol | 平衡时反应中的能量变化 | ||
| N2 | H2 | NH3 | ||
| ① | 1 | 3 | 0 | 放出热量a kJ |
| ② | 2 | 3 | 0 | 放出热量b kJ |
| ③ | 2 | 6 | 0 | 放出热量c kJ |
| A. | N2的转化率:②>①>③ | B. | 三个容器内反应的平衡常数:③>①>② | ||
| C. | 平衡时氨气的体积分数:①>③ | D. | 放出热量关系:2a<c<184.8 kJ |