题目内容
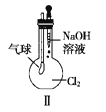
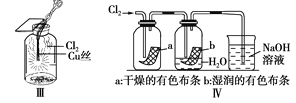
【题目】某同学用下列装置制备并检验Cl2的性质,下列说法正确的是( )

A. Ⅰ图中:如果MnO2过量,浓盐酸就可全部消耗
B. Ⅱ图中:若气球干瘪,证明Cl2可与NaOH反应
C. Ⅲ图中:生成蓝色的烟
D. Ⅳ图中:湿润的有色布条褪色;将硫酸溶液滴入烧杯中,至溶液显酸性,结果有Cl2生成
【答案】D
【解析】A、MnO2只能与浓盐酸反应,因为MnO2是过量,随着反应的进行,盐酸浓度降低,到达某一浓度,反应将会停止,因此MnO2过量时,盐酸不能全部消耗,故A错误;B、Cl2与NaOH反应,造成烧瓶内压强减小,气球鼓起,故B错误;C、Cu和Cl2反应生成棕黄色烟,故C错误;D、干燥氯气不能使干燥的有色布条褪色,能够使湿润的有色布条褪色,Cl2和NaOH反应生成NaCl和NaClO,烧杯中加入硫酸,发生Cl-+ClO-+2H+=Cl2+H2O,故D正确。

 七星图书口算速算天天练系列答案
七星图书口算速算天天练系列答案 初中学业考试导与练系列答案
初中学业考试导与练系列答案【题目】某溶液中,若忽略水的电离,只含有下表中所示的四种离子,推测X离子及其个数b可能为
离子 | Na+ | Al3+ | Cl- | X |
个数 | 3a | 2a | a | b |
A.OH-、8aB.NO3-、4aC.SO42-、4aD.SO42-、8a
【题目】某温度下,在三个容积均为1L的恒容密闭容器中仅发生反应: 2NO(g)+Br2(g)![]() 2NOBr(g)(正反应放热)。下列说法正确的是
2NOBr(g)(正反应放热)。下列说法正确的是
容器 编号 | 物质的起始浓度(mol/L) | 物质的平衡浓度(mol/L) | ||
c(NO) | c(Br2) | c(NOBr) | c(NOBr) | |
I | 0.3 | 0.15 | 0.1 | 0.2 |
II | 0.4 | 0.2 | 0 | |
III | 0 | 0 | 0.2 | |
A. 容器II达平衡所需的时间为4min,则v(Br2)=0.05mol/(Lmin)
B. 达平衡时,容器I与容器III中的总压强之比为2:1
C. 升高温度,逆反应速率增大,正反应速率减小,平衡向逆反应方向移动
D. 达平衡时,容器II中c(Br2)/c(NOBr)比容器III中的小