题目内容
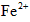 34%~36%,是糖衣片,……,与
34%~36%,是糖衣片,……,与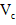 (维生素C)同服可增加本品吸收。某同学设计实验时对其中的铁成分进行了验证。请完成该实验:
(维生素C)同服可增加本品吸收。某同学设计实验时对其中的铁成分进行了验证。请完成该实验:(1)第一步:查阅资料得知,双氧水可以氧化
 生成
生成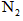 、
、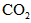 和SO42-,也可以将
和SO42-,也可以将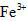 氧化成
氧化成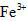 。
。(2)第二步:向去掉糖衣、研磨好的药品中加稀盐酸,出现淡绿色浑浊液,说明有Fe2+离子存在;
(3)第三步:往上述溶液中滴入几滴KSCN溶液,出现浅红色,说明溶液中有少量
 离子存在。该离子存在的原因可能是(填序号):___________________
离子存在。该离子存在的原因可能是(填序号):___________________ ①药品中的铁本来就是以三价铁的形式存在;
②在制药过程中生成少量三价铁;
③本实验过程中有少量三价铁生成。
(4)第四步:将第三步所得溶液分成2份,分别装在A、B两个试管中。
(5)第五步:向A试管的溶液中加入少量稀硫酸,再慢慢滴入过量的
 溶液,溶液的红色先变深,之后红色逐渐褪去。
溶液,溶液的红色先变深,之后红色逐渐褪去。 ①红色变深的原因是(用离子方程式表示):__________________________;
②请自选中学实验室中常用仪器、药品,设计实验证明溶液红色褪去的原因:____________________。
(6)第六步:向B试管的溶液中加入一片
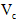 片,片刻后溶液红色也褪去,说明
片,片刻后溶液红色也褪去,说明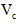 有___________性。
有___________性。II、以石墨为电极,电解法处理黄铜矿(CuFeS2)精矿,可以制得硫酸铜溶液和单质硫。黄铜矿在阳极的浸出反应比较复杂,主要有:CuFeS2 + 4H+ = Cu2+ + Fe2+ + 2H2S,CuFeS2+4Fe3+=Cu2++5Fe2++2S, 2Fe3+ + H2S = 2H+ + S↓ + 2Fe2+。下图为该工艺的示意图。
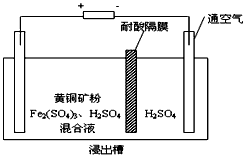
(2)电解过程中阴极有金属析出,向阴极通空气的原因是________________________。
(3)与燃烧法炼铜相比,电解法的优点为________________________。
(3)②③;
(5)①
 ,
, ;
;②取一支试管,加入少量
 溶液和几滴
溶液和几滴 溶液,溶液变为红色,再加入适量
溶液,溶液变为红色,再加入适量 振荡,产生气泡,红色褪去,说明是
振荡,产生气泡,红色褪去,说明是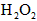 氧化了溶液的
氧化了溶液的 离子使溶液褪色;
离子使溶液褪色;(6)还原性
II、
(1)Fe2+-e-=Fe3+
(2)氧气与硫酸、铜反应生成硫酸铜
(3)不产生二氧化硫污染空气

 走进文言文系列答案
走进文言文系列答案2013年底,上海青浦发生一家三口误食亚硝酸盐造成两男孩身亡的惨剧。常见的亚硝酸盐主要是亚硝酸钠(NaNO2),它是一种白色不透明晶体,虽然形状很像食盐,而且有咸味,但有毒。亚硝酸钠和氯化钠的部分资料如下表:
|
|
亚硝酸钠(NaNO2) |
氯化钠(NaCl) |
|
水溶性 |
易溶,溶液呈弱碱性 |
易溶,溶液呈中性 |
|
熔点 |
271℃ |
801℃ |
|
沸点 |
320℃会分解 |
1413℃ |
|
跟稀盐酸作用 |
有红棕色的NO2气体放出 |
无反应 |
完成下列填空:
(1)氮元素最外层电子排布式为________,氮原子核外电子共占据了___个轨道。亚硝酸钠中各元素原子半径由大到小依次为_________,亚硝酸的电离方程式为:_______________________。
(2)亚硝酸盐中毒是因为亚硝酸盐可将正常的血红蛋白氧化成高铁血红蛋白,即血红蛋白中的铁元素由二价变为三价,失去携氧能力,使组织出现缺氧现象.美蓝是亚硝酸盐中毒后的有效解毒剂.下列说法不正确的是( )
A.高铁血红蛋白的还原性比亚硝酸盐弱
B.药品美蓝应具有还原性
C.中毒时亚硝酸盐发生还原反应
D.解毒时高铁血红蛋白被还原
(3)NaNO2有毒,将含该物质的废水直接排放会引起水体的严重污染,所以这种废水必须处理后才能排放。处理方法之一:在酸性条件下, NaNO2与KI的物质的量为1:1时恰好完全反应,且I-被氧化为I2,此时产物中含氮的物质(A)为________(填化学式)。若利用上述方法制A,现有两种操作步骤:①先将废水酸化后再加KI;②先将KI酸化后再加入废水。哪种方法较好?____(填序号。假设废水中其它物质不反应)
(4)如要鉴别亚硝酸钠和氯化钠固体,下列方法不可行的是
A.观察并比较它们在水中的溶解速度 B.测定它们各自的熔点
C.在它们的水溶液中滴加甲基橙 D.在酸性条件下加入KI淀粉试液
 O2+HbCO,导致人体缺氧。某实验室模拟研究上述过程。
O2+HbCO,导致人体缺氧。某实验室模拟研究上述过程。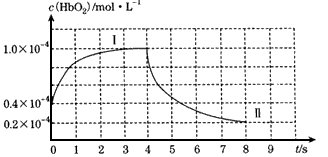
 O2+HbCO的平衡常数的值为____________。
O2+HbCO的平衡常数的值为____________。