题目内容
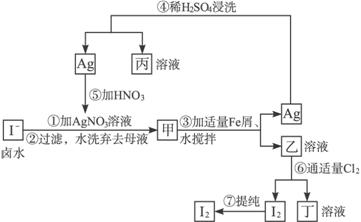
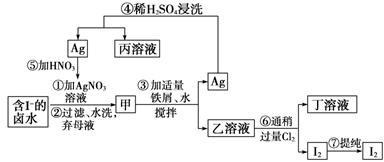
在已经提取氯化钠、溴、镁等化学物质的富碘卤水中,采用下面的工艺流程生产单质碘: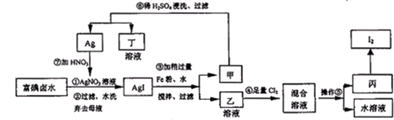
(1)步骤③加Fe粉的目的是
(2)写出步骤④中反应的离子方程式
(3)上述生产流程中,可以循环利用的副产物是
(4)操作⑤的名称是
分析:(1)依据图示流程,过滤水洗后的甲为AgI,加入Fe搅拌,可得Ag和FeI2;
(2)乙溶液为具有还原性的FeI2,向其中通Cl2,氯气氧化碘离子和二价铁离子;
(3)依据流程图可知,Ag(或AgNO3)可循环利用;
(4)利用溶解度的不同进行萃取,分离I2和FeCl3溶液,通常选择萃取剂将碘水中的碘萃取出来.
(2)乙溶液为具有还原性的FeI2,向其中通Cl2,氯气氧化碘离子和二价铁离子;
(3)依据流程图可知,Ag(或AgNO3)可循环利用;
(4)利用溶解度的不同进行萃取,分离I2和FeCl3溶液,通常选择萃取剂将碘水中的碘萃取出来.
解答:解:(1)富碘卤水中含有I-,加入硝酸银发生:Ag++I-═AgI↓,过滤水洗后的甲为AgI,加入Fe搅拌,可得Ag和FeI2,
故答案为:使碘化银转化成碘化亚铁(FeI2)和单质银(或将难溶的碘化银转化成可溶的碘化亚铁);
(2)FeI2具有还原性,与充足的氯气发生氧化还原反应生成I2和FeCl3,反应的化学方程式为2FeI2+3Cl2═2I2+2FeCl3,
故答案为:2Fe2++4I-+3Cl2=2I2+2Fe3++6Cl-;
(3)由流程图可看出,副产物为Ag,由于加入的Fe过量,所以在甲中先加入稀硫酸除去Fe,再加入稀硝酸与Ag反应制得AgNO3溶液,所以Ag(或AgNO3)可循环利用,
故答案为:Ag(或AgNO3);
(4)碘在CCl4中的溶解度大于在水中的溶解度,CCl4和水不互溶,且CCl4和碘不反应,分离I2和FeCl3溶液方法是加入CCl4有机溶剂进行萃取、分液,
故答案为:萃取、分液;CCl4.
故答案为:使碘化银转化成碘化亚铁(FeI2)和单质银(或将难溶的碘化银转化成可溶的碘化亚铁);
(2)FeI2具有还原性,与充足的氯气发生氧化还原反应生成I2和FeCl3,反应的化学方程式为2FeI2+3Cl2═2I2+2FeCl3,
故答案为:2Fe2++4I-+3Cl2=2I2+2Fe3++6Cl-;
(3)由流程图可看出,副产物为Ag,由于加入的Fe过量,所以在甲中先加入稀硫酸除去Fe,再加入稀硝酸与Ag反应制得AgNO3溶液,所以Ag(或AgNO3)可循环利用,
故答案为:Ag(或AgNO3);
(4)碘在CCl4中的溶解度大于在水中的溶解度,CCl4和水不互溶,且CCl4和碘不反应,分离I2和FeCl3溶液方法是加入CCl4有机溶剂进行萃取、分液,
故答案为:萃取、分液;CCl4.
点评:本题考查单质碘的制备,题目难度中等,注意根据物质的性质认真分析流程图的反应过程,正确判断各物质是解答该题的关键.

练习册系列答案
 永乾教育寒假作业快乐假期延边人民出版社系列答案
永乾教育寒假作业快乐假期延边人民出版社系列答案
相关题目