题目内容
【题目】某烯烃与H2发生加成反应后得到的产物是CH3CH(CH3)2.
(1)该产物的系统命名的名称为______,写出该产物的同分异构体的结构简式______
(2)光照条件下,该产物与氯气反应,生成含两个甲基的一氯代物,写出反应的化学方程式______________________ ,反应类型是______________
(3)原来烯烃的结构简式为:______,系统命名的名称为______________
(4)写出该烯烃一定条件下发生加聚反应的方程式:_____________;
(5)写出原来的烯烃使溴的四氯化碳溶液褪色的化学反应方程式:____; 反应类型是__________
【答案】 2-甲基丙烷 CH3CH2CH2CH3 CHCH(CH)CH+Cl→CHCH(CH)CH2Cl+HCl 取代反应 CH2=C(CH)CH 2-甲基-1-丙烯(2-甲基丙烯) n CH2=C(CH3)2 →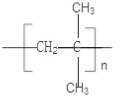 CH2=C(CH3)2+Br2 →CH2Br-CBr(CH3)2 加成反应
CH2=C(CH3)2+Br2 →CH2Br-CBr(CH3)2 加成反应
【解析】(1)CH3CH(CH3)2系统命名的名称为2-甲基丙烷;2-甲基丙烷的同分异构体的结构简式CH3CH2CH2CH3;(2)光照条件下,该产物与氯气反应,生成含两个甲基的一氯代物,反应的化学方程式CH3CH(CH3)CH3+Cl2![]() CH3CH(CH3)CH2Cl+HCl ,反应类型是取代反应;(3)原来烯烃的结构简式为: CH2=C(CH3)2,系统命名的名称为:2-甲基-1-丙烯(2-甲基丙烯);(4)该烯烃一定条件下发生加聚反应的方程式: n CH2=C(CH3)2 →
CH3CH(CH3)CH2Cl+HCl ,反应类型是取代反应;(3)原来烯烃的结构简式为: CH2=C(CH3)2,系统命名的名称为:2-甲基-1-丙烯(2-甲基丙烯);(4)该烯烃一定条件下发生加聚反应的方程式: n CH2=C(CH3)2 →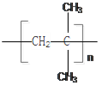 (5)原来的烯烃使溴的四氯化碳溶液褪色的化学反应方程式: CH2=C(CH3)2+Br2 →CH2Br-CBr(CH3)2,属于加成反应。
(5)原来的烯烃使溴的四氯化碳溶液褪色的化学反应方程式: CH2=C(CH3)2+Br2 →CH2Br-CBr(CH3)2,属于加成反应。

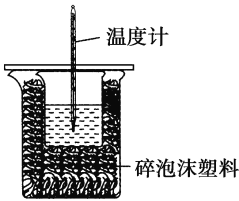
【题目】某实验小组用100 mL 0.50 mol·L-1 NaOH溶液与100 mL 0.55 mol·L-1盐酸进行中和热的测定。装置如图所示。回答下列问题:
(1)若实验共需要400 mL NaOH溶液,实验室在配制该溶液时,则需要称量NaOH固体______g。
(2)图中装置缺少的仪器是______________________________。
(3)盐酸稍过量的原因是________________________________。
(4)碎泡沫塑料及泡沫塑料板的作用是___________________。
(5)若用等浓度的醋酸与NaOH溶液反应,则测得的中和热(ΔH)________(填“偏大”“偏小”或“不变”),其原因是_______。
(6)请填写下表中的平均温度差:
实验次数 | 起始温度T1/℃ | 终止温度 T2/℃ | 平均温度差 (T2-T1)/℃ | |||
HCl | NaOH | 平均值 | ||||
1 | 26.2 | 26.0 | 26.1 | 30.1 | ________ | |
2 | 27.0 | 27.4 | 27.2 | 33.3 | ||
3 | 25.9 | 25.9 | 25.9 | 29.8 | ||
4 | 26.4 | 26.2 | 26.3 | 30.4 | ||
(7)若测得该反应放出的热量为2.865 kJ,请写出盐酸与NaOH溶液反应的中和热的方程式:__________________________________________。