题目内容
向100mL 0.1mol/L的AlCl3溶液中滴加NaOH溶液,当滴加碱液800mL时,恰好完全反应得到澄清的溶液,求NaOH溶液的物质的量浓度.
解:AlCl3的物质的量为0.1L×0.1mol/L=0.01mol,
由恰好完全反应得到澄清的溶液,设NaOH溶液的物质的量浓度为x,则
AlCl3+4NaOH═NaAlO2+3NaCl+H2O
1 4
0.01mol 0.8x
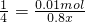 ,解得x=0.05mol/L,
,解得x=0.05mol/L,
答:NaOH溶液的物质的量浓度为0.05mol/L.
分析:根据恰好完全反应得到澄清的溶液,发生AlCl3+4NaOH═NaAlO2+3NaCl+H2O,然后利用n=cV来计算即可.
点评:本题考查物质的量浓度的计算,明确恰好完全反应发生的化学反应是解答本题的关键,然后将物质的物质的量代入化学反应方程式计算即可解答,难度不大.
由恰好完全反应得到澄清的溶液,设NaOH溶液的物质的量浓度为x,则
AlCl3+4NaOH═NaAlO2+3NaCl+H2O
1 4
0.01mol 0.8x
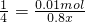 ,解得x=0.05mol/L,
,解得x=0.05mol/L,答:NaOH溶液的物质的量浓度为0.05mol/L.
分析:根据恰好完全反应得到澄清的溶液,发生AlCl3+4NaOH═NaAlO2+3NaCl+H2O,然后利用n=cV来计算即可.
点评:本题考查物质的量浓度的计算,明确恰好完全反应发生的化学反应是解答本题的关键,然后将物质的物质的量代入化学反应方程式计算即可解答,难度不大.

练习册系列答案
相关题目
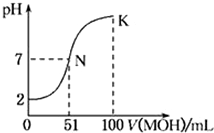 (2013?济南一模)常温下,向100mL 0.01mol?L-1 HA溶液中逐滴加入0.02 mol?L-1 MOH溶液,图中所示的曲线表示混合溶液的pH变化情况(溶液体积变化勿略不计).下列说法中,不正确的是( )
(2013?济南一模)常温下,向100mL 0.01mol?L-1 HA溶液中逐滴加入0.02 mol?L-1 MOH溶液,图中所示的曲线表示混合溶液的pH变化情况(溶液体积变化勿略不计).下列说法中,不正确的是( )
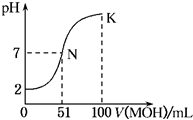 常温下,向100mL 0.01mol?L-1HA溶液中逐滴加入0.02mol?L-1MOH溶液,图中所示曲线表示混合溶液的pH变化情况(体积变化忽略不计).回答下列问题:
常温下,向100mL 0.01mol?L-1HA溶液中逐滴加入0.02mol?L-1MOH溶液,图中所示曲线表示混合溶液的pH变化情况(体积变化忽略不计).回答下列问题: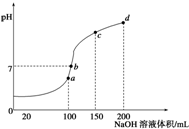 室温时,向100mL 0.1mol/L NH4HSO4溶液中滴加0.1mol/L NaOH溶液,得到溶液pH与NaOH溶液体积的关系曲线如图所示:
室温时,向100mL 0.1mol/L NH4HSO4溶液中滴加0.1mol/L NaOH溶液,得到溶液pH与NaOH溶液体积的关系曲线如图所示: