题目内容
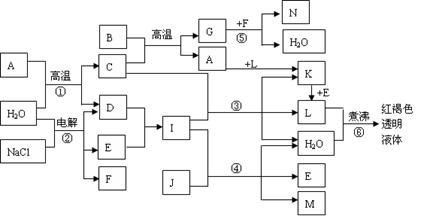
⑴写出化学式:B: ;L:
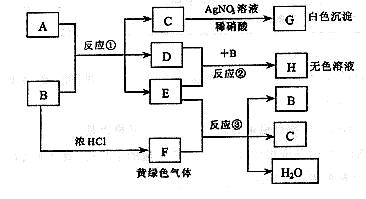
⑵写出反应方程式①
④
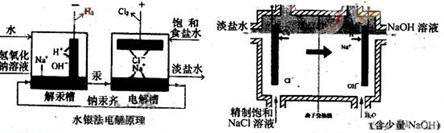
⑶反应②在上世纪七十年代常用水银法替代生产,此法通过钠汞齐(Na·nHg)生产得到的烧碱质量号,浓度高,目前已被离子交换膜法所取代。两种生产方法示意图如下:
下列说法肯定不正确的是 (选填A、B、C、D)
A、水银法被淘汰,可能是时汞毒性大,易造成环境污染
B、水银法在电解槽中,阴极的电极反应式为:Na++e—+nHg== Na·nHg
C、离子膜法电解,阳极发生的电极反应为2H+ + 2e— = H2
D、离子膜法烧碱在阴极生成,水银法烧碱在解汞槽中生成
(每空均2分)(1)Al,FeCl3(2) ;Pb3O4+8HCl==3PbCl2+Cl2+4H2O;(3)BC(4分)
;Pb3O4+8HCl==3PbCl2+Cl2+4H2O;(3)BC(4分)
 ;Pb3O4+8HCl==3PbCl2+Cl2+4H2O;(3)BC(4分)
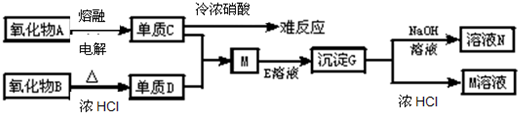
;Pb3O4+8HCl==3PbCl2+Cl2+4H2O;(3)BC(4分)本题将无机框图推断与电解原理的考查有机结合,题型新颖,颇有创意。此框图推断题的突破口是:①J元素+2价比+4价稳定,则J为Pb;②金属A与H2O反应的条件是“高温”,且L+H2O(煮沸)→红褐色透明液体(氢氧化铁胶体),则A为Fe,继而可推出金属B为Al;其余的的物质即可相继推出。(3)水银法阴极的电极反应式为:2H2O+2e-==H2↑+2OH-;离子膜法阳极的电极反应式为:2Cl--2e-==Cl2↑,故B、C错误。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目