题目内容
【题目】高分子材料 M 在光聚合物和金属涂料方面有重要用途,M 的结构简式为
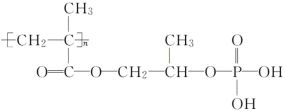
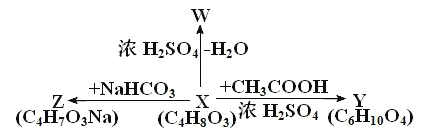
工业上合成 M 的过程可表示如下:
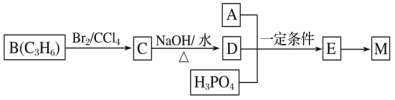
已知:A 完全燃烧只生成 CO2 和 H2O,其蒸汽密度是相同状况下氢气密度的 43 倍,分子中 H、O 原子个数比为 3∶1,它与 Na 或 Na2CO3 都能反应产生无色气体。
(1)B 的结构简式是_____。
(2)A 中所含官能团的名称是_____。
(3)下列说法正确的是_____(填字母)。
a 工业上,B 主要通过石油分馏获得
b C 的同分异构体有 3 种(不包括 C)
c E→M 的反应是缩聚反应
(4)写出 A+D+H3PO4→E 反应的化学方程式:_____。
(5)F 是 A 的一种同分异构体,F 的核磁共振氢谱显示分子中有两种不同的氢原子。存在下列转化关系:
![]()
ⅰ、写出 F、N 的结构简式 F:_____;N:_____。
ⅱ、写出反应①的化学方程式_____。
【答案】CH2=CH-CH3 碳碳双键、羧基 b 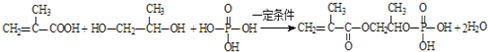 OHC-CH2-CH2-CHO
OHC-CH2-CH2-CHO 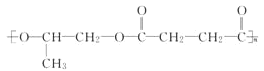 OHC-CH2-CH2-CHO+4[Ag(NH3)2]OH
OHC-CH2-CH2-CHO+4[Ag(NH3)2]OH![]() H4NOOC-CH2-CH2-COONH4+6NH3+2H2O+4Ag
H4NOOC-CH2-CH2-COONH4+6NH3+2H2O+4Ag
【解析】
B为分子式为C3H6,能与溴发生加成反应,则B为CH3CH=CH2,C为CH3CHBrCH2Br,C发生水解反应生成D为![]() .A完全燃烧只生成CO2和H2O,其蒸气密度是相同状况下氢气密度的43倍,Mr(A)=43×2=86,分子中H、O原子个数比为3:1,它与Na或Na2CO3都能反应产生无色气体,说明分子中含有羧基,D与A、H3PO4反应得到E,E转化得到M,结合M的结构简式可知,A为
.A完全燃烧只生成CO2和H2O,其蒸气密度是相同状况下氢气密度的43倍,Mr(A)=43×2=86,分子中H、O原子个数比为3:1,它与Na或Na2CO3都能反应产生无色气体,说明分子中含有羧基,D与A、H3PO4反应得到E,E转化得到M,结合M的结构简式可知,A为![]() ,E为
,E为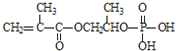 ,(5)中F是A的一种同分异构体,F的核磁共振氢谱显示分子中有两种不同的氢原子,且能发生银镜反应,说明分子中含有-CHO,则F为OHC-CH2-CH2-CHO,被氧化生成H为HOOC-CH2-CH2-COOH,H与D发生缩聚反应生成高聚物N,则N为
,(5)中F是A的一种同分异构体,F的核磁共振氢谱显示分子中有两种不同的氢原子,且能发生银镜反应,说明分子中含有-CHO,则F为OHC-CH2-CH2-CHO,被氧化生成H为HOOC-CH2-CH2-COOH,H与D发生缩聚反应生成高聚物N,则N为 ,据此解答。
,据此解答。
(1)由上述分析可知,B的结构简式为CH3CH=CH2;
(2)由上述分析可知,A为![]() ,含有官能团为:碳碳双键、羧基;
,含有官能团为:碳碳双键、羧基;
(3)a.B为CH3CH=CH2,应通过石油的裂化获得,故a错误;
b.C为CH2BrCHBrCH3,对应的同分异构体有CHBr2CH2CH3、CH3CBr2CH3、CH2BrCH2CH2Br3种(不包括C),故b正确;
c.E→M的反应是加聚反应,故c错误;
故答案为:b;
(4)A+D+H3PO4--E反应的化学方程式为: ,该反应类型是:酯化反应;
,该反应类型是:酯化反应;
(5)ⅰ.F是A的一种同分异构体,F的核磁共振氢谱显示分子中有两种不同的氢原子,且能发生银镜反应,说明分子中含有-CHO,应为OHC-CH2-CH2-CHO,被氧化生成H为HOOC-CH2-CH2-COOH,可与D发生缩聚反应生成N,为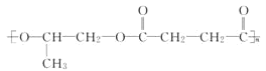 ;
;
ⅱ.反应①的化学方程式为:OHC-CH2-CH2-CHO+4[Ag(NH3)2]OH![]() H4NOOC-CH2-CH2-COONH4+6NH3+2H2O+4Ag。
H4NOOC-CH2-CH2-COONH4+6NH3+2H2O+4Ag。