题目内容
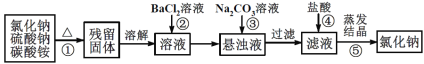
【题目】为了提纯氯化钠固体(混有硫酸钠、碳酸铵杂质),设计了如下实验方案,请回答:
(1)操作①在加热时盛装混合物的仪器可选择__________。
(2)操作②若改为加硝酸钡溶液,对本实验的影响是__________。
(3)进行操作②后,判断SO42-已除尽的方法是__________。
(4)操作③的目的是_____________。
(5)操作⑤蒸发结晶的具体操作为____________。
【答案】坩埚或大试管 引入NO3- 取操作②后的溶液少许于一试管中,静置,往上层清液中维续滴加BaCl2溶液,若不出现浑浊,则SO42-已沉淀完全。 利用碳酸钠除去过量的钡离子 可将溶液置于蒸发皿中,加热蒸发,并用玻璃棒不断搅拌,加热蒸发皿中出现较多固体时,停止加热,利用蒸发皿的余热使滤液蒸干。
【解析】
混有硫酸钠、碳酸铵杂质的氯化钠固体,由流程可知,①中发生加热条件下分解反应,分解后的固体溶于水后,与氯化钡反应除去硫酸根离子,再利用碳酸钠除去过量的钡离子,过滤后滤液中含NaCl、碳酸钠,加盐酸除去碳酸钠后溶质为NaCl,蒸发得到纯净的NaCl。
(1)加热固体,应在坩埚中进行,操作①在加热时盛装混合物的仪器可选择坩埚或大试管。
(2)除杂时不能引入新的杂质,操作②若改为加硝酸钡溶液,对本实验的影响是引入NO3-。
(3)加入过量氯化钡溶液除去硫酸根离子,检验硫酸根离子已全部沉淀,判断方法为取操作②后的溶液少许于一试管中,静置,往上层清液中维续滴加BaCl2溶液,若不出现浑浊,则SO42-已沉淀完全。
(4)操作③的目的是利用碳酸钠除去过量的钡离子。
(5)由氯化钠溶液得到固体氯化钠,操作⑤蒸发结晶的具体操作为:可将溶液置于蒸发皿中,加热蒸发,并用玻璃棒不断搅拌,加热蒸发皿中出现较多固体时,停止加热,利用蒸发皿的余热使滤液蒸干。

【题目】在3个2L的密闭容器中,在相同的温度下、使用相同的催化剂分别进行反应:3H2(g)+N2(g)![]() 2NH3(g),按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时有关数据如下:
2NH3(g),按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时有关数据如下:
容器 | 甲 | 乙 | 丙 |
反应物的投入量 | 3molH2、2molN2 | 6molH2、4molN2 | 2molNH3 |
达到平衡的时间/min | 5 | 8 | |
平衡时N2的浓度/mol·L-1 | c1 | 1.5 | |
NH3的体积分数 | ω1 | ω3 | |
混合气体的密度/g·L-1 | ρ1 | ρ2 |
下列说法正确的是( )
A.2c1<1.5B.ρ1=ρ2
C.ω1=2ω3D.在该温度下甲容器中反应的平衡常数K=![]()