题目内容
已知:2Zn(s)+O2(g)=2ZnO(s) △H="-701.0" kJ?mol-1
2Hg(I)+O2(g)=2HgO(s) △H="-181.6" kJ?mol-1
则反应Zn(s)+HgO(s)=ZnO(s)+Hg(I)的△H为
| A.-519.4kJ?mol-1 | B.+259.7 kJ?mol-1 | C.-259.7 kJ?mol-1 | D.+519.4 kJ?mol-1 |
C
解析试题分析:①2Zn(s)+O2(g)=2ZnO(s) △H="-701.0" kJ?mol-1
②2Hg(I)+O2(g)=2HgO(s) △H="-181.6" kJ?mol-1
由(①-②)/2可求得Zn(s)+HgO(s)=ZnO(s)+Hg(I)的△H为-259.7 kJ?mol-1。故答案C
考点:盖斯定律的应用

 小学课时作业全通练案系列答案
小学课时作业全通练案系列答案 金版课堂课时训练系列答案
金版课堂课时训练系列答案 单元全能练考卷系列答案
单元全能练考卷系列答案 新黄冈兵法密卷系列答案
新黄冈兵法密卷系列答案下列说法正确的是:
A.在100 ℃、101 kPa条件下,1mol液态水气化时需要吸收40.69 kJ的热量,则H2O(g) H2O(l) 的ΔH = +40.69 kJ·mol-1 H2O(l) 的ΔH = +40.69 kJ·mol-1 |
| B.已知CH4 (g)+2O2(g)=CO2(g)+2H2O(l);△H=-802.33kJ/mol,则CH4的燃烧热为802.33 kJ |
C.H2(g)+Br2(g)=2HBr(g)△H=-72kJ·mol-1其它相关数据如下表: 则表中a为230 |
| D.已知S (g)+O2(g)=SO2(s);△H1,S (g)+O2(g)=SO2(g);△H2,则△H2<△H1 |
以下变化后物质的总能量升高的是
| A.钢铁生锈 | B.气态SO3变成固态三聚物 |
| C.水电解 | D.1,3-环己二烯生成苯 |
已知在25℃时:2C(s)+O2(g)=2CO(g) △H1=-222kJ/mol
2H2(g)+O2(g)=2H2O(g) △H2=-484kJ/mol
C(s)+O2(g)=CO2(g) △H3=-394kJ/mol
则25℃时,CO(g)+H2O(g)=CO2(g)+H2(g)的反应热△H4为
| A.-82kJ/mol | B.-41kJ/mol | C.-312kJ/mol | D.+82kJ/mol |
如图是某条件时N2与H2反应过程中能量变化的曲线图。下列叙述正确的是 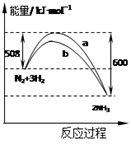
A.该反应的热化学方程式为:2NH3  N2+3H2ΔH =-92 kJ·mol-1 N2+3H2ΔH =-92 kJ·mol-1 |
| B.正反应的活化能小于逆反应的活化能 |
| C.a曲线是加入催化剂时的能量变化曲线 |
| D.加入催化剂可增大正反应速率,降低逆反应速率 |
工业生产水煤气的反应为:C(s)+ H2O(g)=CO(g)+H2(g) ΔH=+131.4 kJ·mol-1,下列判断正确的是( )。
| A.反应物能量总和大于生成物能量总和 |
| B.CO(g)+H2(g)=C(s)+H2O(l) ΔH=-131.4 kJ·mol-1 |
| C.水煤气反应中生成1 mol H2(g)吸收131.4 kJ热量 |
| D.水煤气反应中生成1体积CO(g)吸收131.4 kJ热量 |
如图所示,ΔH1=-393.5 kJ·mol-1,ΔH2=-395.4 kJ·mol-1,下列说法或表示式正确的是( )
| A.C(s、石墨)=C(s、金刚石)ΔH=+1.9 kJ·mol-1 |
| B.石墨和金刚石的转化是物理变化 |
| C.金刚石的稳定性强于石墨 |
| D.1 mol石墨的能量比1 mol金刚石的总能量大 |
下列与化学反应能量变化相关的叙述正确的是 ( )。
| A.生成物总能量一定低于反应物总能量 |
| B.酒精可用作燃料,说明酒精燃烧是释放能量的反应 |
| C.干冰气化需要吸收大量的热,这个变化是吸热反应 |
| D.同温同压下,H2(g)+Cl2(g)===2HCl(g)在光照和点燃条件下的ΔH不同 |
已知:NH3·H2O(aq)与H2SO4(aq)反应生成1 mol正盐的ΔH=
-24.2 kJ·mol-1;强酸、强碱的稀溶液反应的中和热ΔH=-57.3 kJ·mol-1。则NH3·H2O在水溶液中电离的ΔH等于( )
| A.-69.4 kJ·mol-1 | B.-45.2 kJ·mol-1 |
| C.+69.4 kJ·mol-1 | D.+45.2 kJ·mol-1 |