题目内容
铀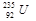 是重要的核工业原料,在自然界中的含量很低。下列有关铀
是重要的核工业原料,在自然界中的含量很低。下列有关铀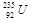 的说法正确的是
的说法正确的是
A.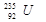 与 与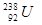 的性质完全相同 的性质完全相同 |
B.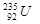 原子核中含有143个中子 原子核中含有143个中子 |
C. 属于短周期元素 属于短周期元素 |
D.1mol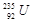 的质量是143g 的质量是143g |
B
解析试题分析: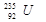 与
与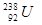 的质子数相同,中子数不同,二者互为同位素,化学性质相似,物理性质不同,A不正确;中子数+质子数=质量数,则
的质子数相同,中子数不同,二者互为同位素,化学性质相似,物理性质不同,A不正确;中子数+质子数=质量数,则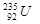 原子核中含有235-92=143个中子,B正确;
原子核中含有235-92=143个中子,B正确; 是锕系元素,位于第七周期,属于长周期元素,C不正确;
是锕系元素,位于第七周期,属于长周期元素,C不正确;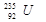 的的相对原子质量近似是235,所以1mol
的的相对原子质量近似是235,所以1mol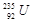 的质量是235g,D不正确,答案选B。
的质量是235g,D不正确,答案选B。
考点:考查同位素的性质、中子数的计算、元素周期表的结构以及质量数的应用等
点评:该题是常识性知识等考查,难度不大。主要是考查学生对原子组成以及组成原子的几种微粒之间数量关系的了解掌握情况,意在培养学生分析、概念和总结问题的能力。

练习册系列答案
相关题目
根据下表部分短周期元素的信息,判断相关叙述正确的是
| 元素代号 | L | M | Q | R | T |
| 原子半径/nm | 0.160 | 0.143 | 0.089 | 0.102 | 0.074 |
| 主要化合价 | +2 | +3 | +2 | +6、-2 | -2 |
A.氢化物的稳定性:H2T<H2R
B.L的金属性比Q强
C.L与T形成的化合物属于离子化合物
D.L和M两者最高价氧化物对应的水化物能相互反应
下列说法正确的是
| A.同一主族相邻两个周期的元素的原子序数差一定等于上一周期所含元素种类 |
| B.短周期元素中某元素的原子序数不可能是同主族元素原子序数的2倍 |
| C.L层上的电子数为奇数的元素一定是主族元素 |
| D.目前使用的长式元素周期表中,最长的周期含36种元素 |
下列元素中,属于第三周期的是
| A.氮 | B.氟 | C.硅 | D.钾 |
XY2是离子化合物,X和Y的离子的电子层结构与氖原子的相同,则X、Y为
| A.Na和Cl | B.K和S | C.Ca和F | D.Mg和F |
下列叙述中,正确的是 ( )
| A.两种微粒,若核外电子排布完全相同,则其化学性质一定相同 |
| B.凡单原子形成的离子,一定具有稀有气体元素原子的核外电子排布 |
| C.两原子,如果核外电子排布相同,则一定属于同种元素 |
| D.阴离子的核外电子排布一定与上一周期稀有气体元素原子的核外电子排布相同 |
X元素最高氧化物对应的水化物为H3XO4,则它对应的气态氢化物为
| A.XH4 | B.XH3 | C.H2X | D.HX |
短周期元素X,Y,Z在周期表中的位置如图所示,则下列说法中错误的是( )
| | | X |
| | Y | |
| Z | | |
A.X,Y,Z中X的单质最稳定 B.Y的氢化物为HY
C.X能生成HXO D.能发生Cl2+H2Z=Z+2HCl的反应
短周期元素X、Y、Z、W的原子序数依次增大,X原子的最外层电子数是其内层电子总数的3倍,Y原子的最外层只有2个电子,Z单质可制成半导体材料,W与X属于同一主族。下列叙述正确的是( )
| A.原子半径的大小顺序: Y<Z<W<X |
| B.化合物YX、ZX2、WX3中化学键的类型相同 |
| C.非金属性的强弱顺序:X>W>Z |
| D.元素W的最高价氧化物对应水化物的酸性比Z的弱 |