题目内容
【题目】铅蓄电池是历史悠久、用量非常大的蓄电池,其构造图如图所示,放电时有PbSO4生成。
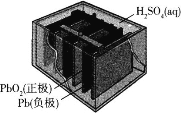
下列说法中错误的是
A.铅蓄电池是二次电池
B.放电时负极电极式:Pb-2e- +SO42-= PbSO4
C.充电时电解质溶液密度增大
D.当电路中转移电子数目为2NA时,溶液中SO42-减少或增加1 mol
【答案】D
【解析】
放电时铅是负极,发生失电子的氧化反应,其电极电极式:Pb-2e- +SO42-= PbSO4;PbO2是正极,发生得电子的还原反应,其电极反应式为:PbO2 + 4H+ + SO42-+2e-= PbSO4+2H2O,电池的总反应可表示为:Pb+PbO2+2H2SO4![]() 2PbSO4+2H2O,充电过程是放电过程的逆过程,据此分析作答。
2PbSO4+2H2O,充电过程是放电过程的逆过程,据此分析作答。
根据上述分析可知,
A. 铅蓄电池可多次放电、充电,是二次电池,A项正确;
B. 放电时铅是负极,负极电极式:Pb-2e- +SO42-= PbSO4,B项正确;
C. 充电时生成硫酸,硫酸的浓度增大,电解质溶液的密度增大,C项正确;
D. 根据总反应式可知,当电路中转移电子数目为2NA时,溶液中SO42-减少或增加2 mol,D项错误;
答案选D。

练习册系列答案
相关题目
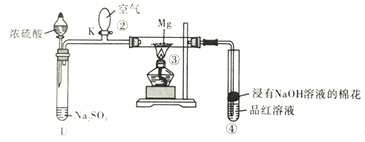
【题目】用下图所示装置检验乙烯时不需要除杂的是( )

乙烯的制备 | 试剂X | 试剂Y | |
A | CH3CH2Br与NaOH乙醇溶液共热 | 水 | Br2的CCl4溶液 |
B | CH3CH2Br与NaOH乙醇溶液共热 | 水 | KMnO4酸性溶液 |
C | C2H5OH与浓H2SO4 | NaOH溶液 | KMnO4酸性溶液 |
D | C2H5OH与浓H2SO4 | NaOH溶液 | Br2的CCl4溶液 |