题目内容
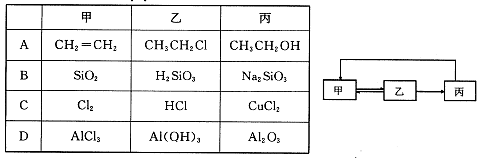
下列物质转化在给定条件下能实现的是
①Al2O3 NaAlO2(aq)
NaAlO2(aq) 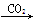 Al(OH)3
Al(OH)3
②S SO3
SO3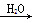 H2SO4
H2SO4
③饱和NaCl(aq) 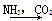 NaHCO3
NaHCO3 Na2CO3
Na2CO3
④Fe2O3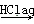 FeCl3(aq)
FeCl3(aq)  无水FeCl3
无水FeCl3
⑤MgCl2(aq)  Mg(OH)2
Mg(OH)2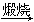 MgO
MgO
| A.①③⑤ | B.②③④ | C.②④⑤ | D.①④⑤ |
A
解析试题分析:①Al2O3+2NaOH=2NaAlO2+2H2O;NaAlO2+H2O+CO2= Al(OH)3↓+ NaHCO3。正确。②S+ O2 SO2,不能反应直接得到SO3.错误。③NaCl+H2O+CO2+NH3= NaHCO3↓+ NH4Cl;2NaHCO3
SO2,不能反应直接得到SO3.错误。③NaCl+H2O+CO2+NH3= NaHCO3↓+ NH4Cl;2NaHCO3 Na2CO3+CO2↑+H2O.正确。④Fe2O3 +6HCl=2FeCl3+3H2O;FeCl3溶液加热最终达到的固体为Fe(OH)3.错误。⑤MgCl2+Ca(OH)2=CaCl2+Mg(OH)2↓. Mg(OH)2
Na2CO3+CO2↑+H2O.正确。④Fe2O3 +6HCl=2FeCl3+3H2O;FeCl3溶液加热最终达到的固体为Fe(OH)3.错误。⑤MgCl2+Ca(OH)2=CaCl2+Mg(OH)2↓. Mg(OH)2 H2O+MgO。正确。因此在物质转化中在给定条件下能实现的是①③⑤。选项为A。
H2O+MgO。正确。因此在物质转化中在给定条件下能实现的是①③⑤。选项为A。
考点:考查物质的化学性质的知识。

向盛有一定量氢氧化钠溶液的烧杯中通入标准状况下448mL氮气和二氧化碳的混合气体后得到溶液A,在溶液A中逐滴加入0.1mol/L的稀盐酸至过量,并将溶液加热,产生的二氧化碳气体的物质的量与加入稀盐酸的体积的关系如图所示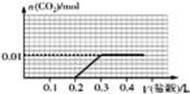
(忽略二氧化碳的溶解和氯化氢的挥发).下列说法正确的是
| A.原混合气体中氮气与二氧化碳体积之比为1:4 |
| B.在逐滴加入稀盐酸产生二氧化碳之前,发生的离子反应为CO32-+H+═HCO3- |
| C.溶液A中含有0.01molNaOH和0.01molNa2CO3 |
| D.当加入0.1L稀盐酸时,此时溶液中离子浓度大小关系为 |
实验:①向盛有1 mL 0.1 mol/L MgCl2溶液试管中加1 mL 0.2 mol/L NaOH溶液,得到浊液a,过滤得到滤液b和白色沉淀c。②向沉淀c中滴加0.1mol/LFeCl3溶液,沉淀变为红褐色。下列分析不正确的是
A.浊液a中存在沉淀溶解平衡:Mg (OH) 2(s) Mg2+(aq)+2OH-(aq) Mg2+(aq)+2OH-(aq) |
| B.滤液b中不含有Mg2+ |
| C.②中颜色变化说明Mg (OH)2转化为Fe(OH)3 |
| D.实验可以证明Fe(OH)3比Mg (OH)2更难溶 |
下列有关物质的性质与应用不踿 相对应的是
| A.明矾能水解生成Al(OH)3胶体,可用作净水剂 |
| B.FeCl3溶液能与Cu 反应,可用于蚀刻印刷电路 |
| C.SO2具有氧化性,可用于漂白纸浆 |
| D.Zn 具有还原性和导电性,可用作锌锰干电池的负极材料 |
下列实验操作中,仪器一定需要插入液面以下的是
①制备Fe(OH)2时将NaOH溶液滴入FeSO4溶液中所用的胶头滴管
②制备氢气的简易装置中的长颈漏斗
③分馏石油时控制温度的温度计
④用乙醇制备乙烯时所用的温度计
⑤向BaCl2溶液中滴加稀硫酸所用的胶头滴管
| A.③⑤ | B.②⑤ | C.①②④ | D.①②③④⑤ |
下列有关金属及其化合物的说法正确的是
| A.Mg和Al都可以用电解法冶炼得到 |
| B.Na2O2、Na2O组成元素相同,与CO2反应产物也相同 |
| C.用过量的KSCN溶液除去FeCl2溶液中的少量FeCl3 |
| D.Mg和Fe在一定条件下与水反应都生成H2和对应的碱 |
美、德两国成功合成具有化学特性的氢铝化合物(AlH3)n,关于氢铝化合物的推测不正确的是 ( )。
| A.氢铝化合物与水反应生成氢氧化铝和氢气 |
| B.氢铝化合物中铝显+3价,氢显-1价 |
| C.铝与水蒸气在高温下反应可生成氢铝化合物 |
| D.氢铝化合物具有强还原性 |