题目内容
2.人类的生产生活离不开金属材料,金属及金属材料在生产、生活中应用广泛.(1)生活中常用的铁锅炒菜,主要是利用了铁的导热性;铁在潮湿的空气中容易锈蚀,喷漆可以延缓汽车钢铁外壳的锈蚀,起防锈原理是隔绝氧气和水,喷漆前需将铁制品放入稀盐酸中除锈(铁锈主要成分是Fe2O3),观察到溶液变黄,有无色气泡逸出,写出其中涉及到的一个化学方程式:Fe2O3+6HCl=2FeCl3+3H2O.
(2)化学实验室要从含少量铜粉的银、锰(Mn)混合金属粉末中分离出贵金属,并获得一种盐晶体,将有关三种金属随意编号为:A、B、C,并设计了如下流程:
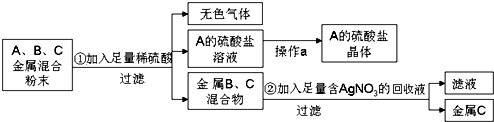
①A、B、C三种金属的活动性顺序为A>B>C.
②金属C是Ag,已知A的硫酸盐中A元素显+2价,请写出步骤①的反应的化学方程式:Mn+H2SO4=MnSO4+H2↑.
分析 (1)铁具有良好的导热性;铁具有强的还原性,遇到氧气、水发生氧化还原反应而被腐蚀;氧化铁能与盐酸反应生成氯化铁和水;
(2)根据金属活动性顺序判断金属是否与酸反应、金属是否能与盐溶液的反应.
解答 解:(1)生活中常用的铁锅炒菜,主要是利用了铁的良好的导热性;潮湿的空气中含义氧气、水,能够氧化铁而使铁发生腐蚀,汽车钢铁外壳喷漆隔绝氧气和水,减缓铁的腐蚀;氧化铁能与盐酸反应生成氯化铁和水,方程式:Fe2O3+6HCl=2FeCl3+3H2O;
故答案为:导热性;氧气和水;Fe2O3+6HCl=2FeCl3+3H2O;
(2)铜、银、锰(Mn)的混合粉末中只有A能与稀硫酸反应生成无色气体和A的盐溶液,所以我们判断A是Mn;金属B、C为铜和银;B、C的混合物加入足量的含硝酸银溶液中,过滤后得到金属C,说明金属C不能与硝酸银溶液反应,金属B能与硝酸银溶液反应,B是Cu,C是银,
①依据活泼性强的金属能够置换活泼性弱的金属,所以:A、B、C三种金属的活动性顺序:A>B>C;
故答案为:A>B>C;
②步骤②的反应是铜和硝酸银反应生成硝酸铜和银,所以C是银;
已知A的硫酸盐中A元素显+2价,硫酸根显-2价,又因为金属A我们已得知是Mn,所以A的硫酸盐的化学式是MnSO4,锰和硫酸反应生成硫酸锰和氢气,化学方程式为:Mn+H2SO4=MnSO4+H2↑;
故答案为:Ag; Mn+H2SO4=MnSO4+H2↑;
点评 本题通过工业分离银的流程考查了金属的性质,明确金属活动性顺序是解题关键,题目难度中等.

练习册系列答案
相关题目
13.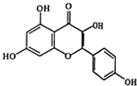 山萘酚(Kaempferol)结构如图所示,且大量存在于水果、蔬菜、豆类、茶叶中,具有多种生物学作用,如抗氧化、抑制肿瘤生长及保护肝细胞等作用.有关山萘酚的叙述正确的是( )
山萘酚(Kaempferol)结构如图所示,且大量存在于水果、蔬菜、豆类、茶叶中,具有多种生物学作用,如抗氧化、抑制肿瘤生长及保护肝细胞等作用.有关山萘酚的叙述正确的是( )
 山萘酚(Kaempferol)结构如图所示,且大量存在于水果、蔬菜、豆类、茶叶中,具有多种生物学作用,如抗氧化、抑制肿瘤生长及保护肝细胞等作用.有关山萘酚的叙述正确的是( )
山萘酚(Kaempferol)结构如图所示,且大量存在于水果、蔬菜、豆类、茶叶中,具有多种生物学作用,如抗氧化、抑制肿瘤生长及保护肝细胞等作用.有关山萘酚的叙述正确的是( )| A. | 结构式中含有2个苯环和羟基、醚键、羧基、碳碳双键 | |
| B. | 可发生取代反应、水解反应、加成反应 | |
| C. | 可与NaOH反应,不能与NaHCO3反应 | |
| D. | 1mol山萘酚与溴水反应最多可消耗4molBr2 |
10.三氟化氮(NF3)气体在潮湿的环境中能发生如下反应:3NF3+5H20=2N0+HNO3+9HF.下列有关该反应的说法正确的是( )
| A. | NF既是氧化剂,又还原剂 | |
| B. | 还原剂与氧化剂的物质的量之比为1:2 | |
| C. | 若生成2molHNO3,则转移2mol电子 | |
| D. | NF3中氢元素的化合价为+3 |
17.下列有关物质燃烧现象的叙述中,正确的是( )
| A. | 铁丝在氧气中燃烧:火星四射,生成红色固体 | |
| B. | 硫粉在空气中燃烧:产生淡蓝色火焰,生成一种刺激性气味的气体 | |
| C. | 镁条在空气中燃烧:发出耀眼的白光,只生成一种黑色固体 | |
| D. | 红磷在空气中燃烧:发出白光,生成大量的白色烟雾 |
7.某中学化学兴趣小组为了测定某矿山石灰石中碳酸钙的质量分数,取石灰石样品与足量的10%的稀盐酸在烧杯中反应(假设石灰石样品中杂质不与稀盐酸反应也不溶于水).有关实验数据如下表:
请计算(写出计算过程):
(1)该石灰石中碳酸钙的质量分数;
(2)参加反应10%的盐酸的质量.
| 反应前 | 反应后 | ||
| 实验 数据 | 烧杯和稀盐酸的质量 | 石灰石样品的质量 | 烧杯和其中混合物的质量 |
| 134.4g | 10g | 141.1g | |
(1)该石灰石中碳酸钙的质量分数;
(2)参加反应10%的盐酸的质量.
14.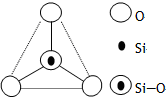 如图所示某硅氧离子的空间结构示意图(虚线不表示共价键).通过观察分析,下列叙述正确的是( )
如图所示某硅氧离子的空间结构示意图(虚线不表示共价键).通过观察分析,下列叙述正确的是( )
 如图所示某硅氧离子的空间结构示意图(虚线不表示共价键).通过观察分析,下列叙述正确的是( )
如图所示某硅氧离子的空间结构示意图(虚线不表示共价键).通过观察分析,下列叙述正确的是( )| A. | 键角为120℃ | B. | 化学组成为SiO32- | ||
| C. | 键角为60° | D. | 化学组成为SiO44- |
12.aXm+、bYn+、cZn-、dRm-四种离子的核外电子排布相同,且m>n、则下列关系正确的是( )
| A. | a-c=m-n | B. | b-d=m+n | C. | a>b>d>c | D. | b>a>c>d |

 ②N2
②N2 ③H2O
③H2O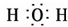 .
.