题目内容
3.①丁烷 ②2-甲基丙烷 ③正戊烷 ④2-甲基丁烷 ⑤2,2-二甲基丙烷等物质的沸点排列顺序正确的是( )| A. | ①>②>③>④>⑤ | B. | ③>④>⑤>①>② | C. | ⑤>④>③>②>① | D. | ②>①>⑤>④>③ |
分析 烃类物质中,烃含有的C原子数目越多,相对分子质量越大,熔沸点越高,同分异构体分子中,烃含有的支链越多,分子间的作用力越小,熔沸点越小.
解答 解:由烷烃中碳原子个数越多,沸点越大,则沸点戊烷>丁烷;同分异构体中支链越多,沸点越低,则2,2-二甲基丙烷<2-甲基丁烷<戊烷,2-甲基丙烷<丁烷,
故沸点大小顺序为:正戊烷>2-甲基丁烷>2,2-二甲基丙烷>丁烷>2-甲基丙烷,即:③>④>⑤>①>②,
故选B.
点评 本题主要考查烷烃沸点高低比较,题目难度不大,关键要掌握烷烃的沸点规律:随碳原子数的增多而升高,碳原子数相同时,支链越多,沸点越低.

练习册系列答案
 科学实验活动册系列答案
科学实验活动册系列答案
相关题目
13.NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A. | 0.1 mol甲烷含有的电子数为NA | |
| B. | 1 L 0.1 mol/L Na2CO3溶液中含有的CO32-数目为0.1 NA | |
| C. | 1 L pH=1的硫酸溶液中含有的H+数为0.2 NA | |
| D. | 1 mol•L-1 FeCl3溶液中所含Cl-的数目为3NA |
14.金刚石和石墨是碳元素的两种结构不同的单质(同素异形体).在100kPa时,1mol金刚石转化为石墨,会放出1.895kJ的热量.据此,试判断在100kPa压强下,下列结论正确的是( )
| A. | 1mol石墨比1mol金刚石的总能量低 | |
| B. | 1mol石墨比1mol金刚石的总能量高 | |
| C. | 金刚石比石墨稳定 | |
| D. | 无法判断石墨和金刚石的相对稳定性 |
11.有关能量的判断或表示方法正确的是( )
| A. | 由H+(aq)+OH-(aq)═H2O(l)△H=-57.3 kJ•mol-1,可知:含0.5 mol H2SO4的浓溶液与含1 mol NaOH的溶液混合,放出热量大于57.3 kJ | |
| B. | 从C(石墨)═C(金刚石)△H=+1.19 kJ•mol-1,可知:金刚石比石墨更稳定 | |
| C. | 等质量的硫蒸气和硫固体分别完全燃烧,后者放出热量更多 | |
| D. | 2 g H2完全燃烧生成液态水放出285.8 kJ热量,则氢气燃烧的热化学方程式为:2H2(g)+O2(g)═2H2O(l)△H=-285.8 kJ•mol-1 |
18.下列有关物质用途的说法错误的是( )
| A. | Na2O2可用作潜水艇的供氧剂 | B. | 水玻璃可用作木材的防火剂 | ||
| C. | 漂白粉可用作自来水的消毒剂 | D. | SO2可用作食品的漂白剂 |
8.已知短周期元素的离子aA2+、bB+、cC3-、dD-都具有相同的电子层结构,则下列叙述正确的是( )
| A. | 原子半径A>B>D>C | B. | 原子序数d>c>b>a | ||
| C. | 离子半径C3->D->B+>A2+ | D. | a=c-5 |
15.由短周期两种元素形成化合物A2B3,A3+比B2-少一个电子层,且A3+具有与Ne原子相同的核外电子层结构,下列说法不正确的是( )
| A. | A2B3是三氧化二铝 | B. | A3+与B2-最外层上的电子数相同 | ||
| C. | A是第3周期第ⅢA族的元素 | D. | B是第3周期第ⅥA族的元素 |
13.“结构决定性质”,有关物质结构的下列说法中正确的是( )


| A. | 碘熔化破坏了共价键 | |
| B. | 从石墨剥离得石墨烯(如右图)需克服范德华力 | |
| C. | 含极性键的共价化合物一定是电解质 | |
| D. | HF的分子间作用力大于HCl,故氟化氢比氯化氢更稳定 |
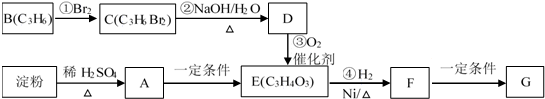
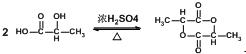 .
.