题目内容
【题目】将镁条、铝条平行插入盛有一定浓度的NaOH溶液的烧杯中,用导线和电流表连接成原电池,装置如图所示。此电池工作时,下列叙述正确的是( )
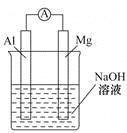
A. Mg比Al活泼,Mg失去电子被氧化成Mg2+
B. 铝条表面虽有氧化膜,但可不必处理
C. 该电池的内外电路中,电流均是由电子定向移动形成的
D. Al是电池负极,开始工作时溶液中会立即有白色沉淀析出
【答案】B
【解析】试题A.在NaOH溶液中,铝能与NaOH溶液发生氧化还原反应,在该反应中,铝失电子作原电池的负极,而属镁和氢氧化钠溶液不能发生氧化还原反应,错误;B.由于铝片表面的氧化膜也能与NaOH溶液反应,故其不必处理,正确;C.该装置外电路,是由电子的定向移动形成电流,而内电路,则是由溶液中自由移动的离子的定向移动形成电流,错误;D.在NaOH溶液中,铝能与NaOH溶液发生氧化还原反应,在该反应中,铝失电子作原电池的负极,由于电池开始工作时,生成的铝离子的量较少,NaOH过量,此时不会有Al(OH)3白色沉淀生成,错误。

 阅读快车系列答案
阅读快车系列答案【题目】在研究化学反应中的能量变化时,我们通常做下面的实验:在一个小烧杯里,加入20克已研磨成粉末的八水合氢氧化钡,将小烧杯放在事先已滴有3-4滴水的玻璃片(或三合板)上,然后向烧杯内加入约10克氯化铵晶体,根据实验步骤,填写下表,并回答问题
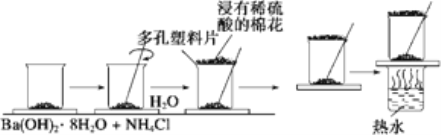
实验步骤 | 实验现象及结论 |
将晶体混合,立即快速搅拌 | 有刺激性气味能使湿润的紫色石蕊试纸变蓝的_______产生(1) |
用手摸烧杯下部 | 感觉烧杯变凉说明此反应是_________反应(2) |
用手拿起烧杯 | 烧杯下面的带有几滴水的玻璃片粘到了烧杯底部 |
将粘有玻璃片的烧杯放在盛有热水的烧杯上 | 玻璃片脱离上面烧杯底部 |
反应后移走多孔塑料片观察反应物 | 混合物成糊状,证明有________生成(3) |
(4)写出实验过程中发生反应的化学方程式__________。
(5)实验中要立即用玻璃棒迅速搅拌的原因是:_________________。
(6)该反应在常温下就可进行,说明_________。