题目内容
【题目】X、Y、Z、R、Q、M是六种短周期元素,原子序数依次增大![]() 是原子半径最小的元素,Y的气态氢化物能使湿润的红色石蕊试纸变蓝,Z为地壳中含量最多的元素,R与X同主族;Y、R、Q最外层电子数之和为8,M的单质黄绿色有害气体
是原子半径最小的元素,Y的气态氢化物能使湿润的红色石蕊试纸变蓝,Z为地壳中含量最多的元素,R与X同主族;Y、R、Q最外层电子数之和为8,M的单质黄绿色有害气体![]() 请回答下列问题:
请回答下列问题:
(1)![]() 在元素周期表中的位置为______.
在元素周期表中的位置为______.
(2)![]() 、Q、M简单离子半径由大到小的顺序为
、Q、M简单离子半径由大到小的顺序为![]() 写元素离子符号
写元素离子符号![]() ______.
______.
(3)![]() 、Y、Z三种元素形成盐类化合物的水溶液呈酸性的原因:
、Y、Z三种元素形成盐类化合物的水溶液呈酸性的原因:![]() 用离子方程式表示
用离子方程式表示![]() ______
______![]() 溶液中所含离子浓度由大到小的顺序为______.
溶液中所含离子浓度由大到小的顺序为______.
(4)![]() 的电子式为______,
的电子式为______,![]() 与水可剧烈反应,产生沉淀与气体,反应的化学方程式为______.
与水可剧烈反应,产生沉淀与气体,反应的化学方程式为______.
(5)![]() 、Z两元素形成的原子个数比为1:1的化合物中含有的化学键类型为______.
、Z两元素形成的原子个数比为1:1的化合物中含有的化学键类型为______.
(6)![]() 的单质与R的最高价氧化物对应的水化物反应的离子方程式为______.
的单质与R的最高价氧化物对应的水化物反应的离子方程式为______.
【答案】 第三周期第IA族 Cl>O2>Mg2+ NH4++H2ONH3H2O+H+ c(NO3)>c(NH4+)>c(H+)>c(OH) 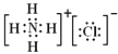 Mg3N2+6H2O=3Mg(OH)2+2NH3↑ 共价键 Cl2+2OH=Cl+ClO+H2O
Mg3N2+6H2O=3Mg(OH)2+2NH3↑ 共价键 Cl2+2OH=Cl+ClO+H2O
【解析】X、Y、Z、R、Q、M是六种短周期元素,原子序数依次增大.X是原子半径最小的元素,故X为H元素;Y的气态氢化物能使湿润的红色石蕊试纸变蓝,故为氨气,则Y为N元素;Z为地壳中含量最多的元素,故为O元素;R与X同主族,且原子序数大于8,故R为Na元素;Y、R、Q最外层电子数之和为8,故Q的最外层有2个电子,且原子序数比11大,故为Mg元素;M的单质黄绿色有害气体,故为Cl元素。
(1)R为Na元素,在周期表中处于第三周期第IA族,故答案为:第三周期第IA族;
(2)Z、Q、M简单离子分别为O2、Mg2+、Cl,而微粒的电子层数越多,则半径越大,故Cl的半径最大;当电子层数相同时,核电荷数越多,则半径越小,故Mg2+的半径最小,故简单离子半径由大到小的顺序为Cl>O2>Mg2+,故答案为:Cl>O2>Mg2+;
(3)X、Y、Z三种元素形成盐类化合物为NH4NO3,NH4+水解显酸性:NH4++H2ONH3H2O+H+,由于NH4+水解,且溶液显酸性,故离子浓度大小为:c(NO3)>c(NH4+)>c(H+)>c(OH),故答案为:NH4++H2ONH3H2O+H+ ;c(NO3)>c(NH4+)>c(H+)>c(OH);
(4)YX4M为NH4Cl,为离子化合物,电子式为:![]() ;Q3Y2为Mg2N3,在水溶液中发生双水解生成氢氧化镁和氨气,反应的化学方程式为:Mg3N2+6H2O=3Mg(OH)2+2NH3↑;故答案为:
;Q3Y2为Mg2N3,在水溶液中发生双水解生成氢氧化镁和氨气,反应的化学方程式为:Mg3N2+6H2O=3Mg(OH)2+2NH3↑;故答案为:![]() ; Mg3N2+6H2O=3Mg(OH)2+2NH3↑;
; Mg3N2+6H2O=3Mg(OH)2+2NH3↑;
(5)X、Z两元素形成的原子个数比为1:1的化合物为H2O2,为共价化合物,只含共价键,故答案为:共价键;
(6)M的单质即为氯气,与R的最高价氧化物对应的水化物即为NaOH反应,生成氯化钠、次氯酸钠和水,离子方程式为:Cl2+2OH=Cl+ClO+H2O,故答案为:Cl2+2OH=Cl+ClO+H2O

 夺冠金卷全能练考系列答案
夺冠金卷全能练考系列答案


