题目内容
(2分)将质量分数为98%,密度为1.84 g·cm-3的浓硫酸,用蒸馏水稀释到9.2 mol/L的硫酸,则其质量分数 49%(填>、<、=)。
>
因为硫酸溶液的密度是随浓度的增大而增大的,所以根据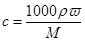 可知,当用蒸馏水稀释到9.2 mol/L时,溶液的质量分数大于49%。
可知,当用蒸馏水稀释到9.2 mol/L时,溶液的质量分数大于49%。
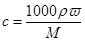 可知,当用蒸馏水稀释到9.2 mol/L时,溶液的质量分数大于49%。
可知,当用蒸馏水稀释到9.2 mol/L时,溶液的质量分数大于49%。
练习册系列答案
相关题目
题目内容
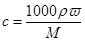 可知,当用蒸馏水稀释到9.2 mol/L时,溶液的质量分数大于49%。
可知,当用蒸馏水稀释到9.2 mol/L时,溶液的质量分数大于49%。