题目内容
【题目】化学科学的发展离不开物质结构的探索和研究。物质结构研究对于保护生态环境、实现社会的可持续发展有重要的意义。请回答下列问题:
(1)基态铜原子最外层电子所占用能级的电子云轮廓图形状为_____,基态硒原子的价电子排布图为____。
(2)次氯酸分子的VSEPR模型名称为_______,中心原子的杂化类型为_________。
(3)C、O、F三者的第一电离能由小到大的顺序为___________。
(4)CaO的熔点比BaO(填“高”或“低”),原因是______。
(5)H2SeO4的酸性比H2SeO3强,原因是_________。
(6)与CN-互为等电子体的离子有________(写出一种即可)。
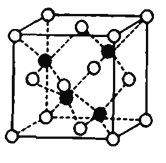
(7)Fe和S形成的某种晶胞如图所示:其中白球表示S,黑球表示Fe,则该物质的化学式为_______.该晶胞中硫原子的配位数为_______;假设该晶胞的密度为ρg/cm3,用NA表示阿伏加德罗常数,则该晶胞中距离最近的S原子之间的距离为__________pm.
【答案】 球形 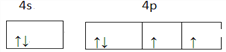 四面体型 sp3 杂化 C<O<F 高,Ca2+ 半径比Ba2+小,CaO的晶格能比BaO大 H2SeO4 和H2SeO3 可用(HO)mSeOn, H2SeO4 中的n值大,Se的正电性高导致Se-O-H中O的电子向Se偏移,在水分子的作用下更容易电离出H + ,所以酸性更强(或者说H2SeO4 中非羟基氧数目多,所以酸性更强也得分) O22+ 或 C22- FeS 4
四面体型 sp3 杂化 C<O<F 高,Ca2+ 半径比Ba2+小,CaO的晶格能比BaO大 H2SeO4 和H2SeO3 可用(HO)mSeOn, H2SeO4 中的n值大,Se的正电性高导致Se-O-H中O的电子向Se偏移,在水分子的作用下更容易电离出H + ,所以酸性更强(或者说H2SeO4 中非羟基氧数目多,所以酸性更强也得分) O22+ 或 C22- FeS 4 ![]() ×1010
×1010
【解析】(1)基态Cu原子核外有4个电子层,最高能层为第四层,即N层,最外层电子为4s1电子,该能层电子的电子云轮廓图形状为球形,硒为34号元素,有6个价电子,所以硒的价层电子排布式为4s24p4,价层电子排布图为![]() 故答案为:球形;
故答案为:球形;![]() ;
;
(2)次氯酸分子中中心原子O有2对孤对电子和2个σ键,VSEPR模型为四面体,O原子采取sp3杂化,故答案为:四面体;sp3杂化;
(3)同一周期中,元素的第一电离能随着原子序数的增大而增大,所以C、O、F元素第一电离能为C<O<F, 故答案为:C<O<F;
(4)离子晶体中离子半径越小,则离子键键能越大,其晶体的晶格能越大,熔点越高,已知钙离子半径小于钡离子半径,所以CaO的熔点高于BaO,故答案为:高;Ca2+ 半径比Ba2+小,CaO的晶格能比BaO大;
(5)H2SeO4中非羟基氧数目多,所以酸性更强,即H2SeO4的酸性比H2SeO3强,故答案为:H2SeO4中非羟基氧数目多,所以酸性更强;
(6)将CN-中C原子及1个负电荷换成1个N原子,可得等电子体N2,将N原子及1个负电荷换成1个O原子,可得等电子体CO,同理互为等电子体的离子有O22+或C22-等,故答案为:O22+(或C22-);
(7)黑球铁处于晶胞内部,晶胞中含有4个Fe原子,白球S处于顶点和面心,晶胞中含有S原子数目为6×![]() +8×
+8×![]() =4,约成最简整数比既得化学式为FeS,根据图示,每个铁原子周围有四个硫原子,即晶胞中铁原子的配位数为4,则硫原子的配位数也为4;晶胞质量为4×
=4,约成最简整数比既得化学式为FeS,根据图示,每个铁原子周围有四个硫原子,即晶胞中铁原子的配位数为4,则硫原子的配位数也为4;晶胞质量为4×![]() g,假设该晶胞的边长为a cm,则(a cm)3×ρ g/cm3=4×
g,假设该晶胞的边长为a cm,则(a cm)3×ρ g/cm3=4×![]() g,则a=
g,则a=![]() ,距离最近的S原子之间距离为晶胞边长的
,距离最近的S原子之间距离为晶胞边长的![]() ,故S原子之间距离为
,故S原子之间距离为![]() ×
×![]() cm=
cm=![]() ×
×![]() ×1010pm,故答案为:FeS;4;
×1010pm,故答案为:FeS;4;![]() ×
×![]() ×1010。
×1010。

【题目】向四只盛有相同量NaOH溶液的烧杯中通入不同量的CO2气体,在所得溶液中逐滴加入稀盐酸至过量,并将溶液加热,产生的CO2气体与HCl物质的量的关系如图:(忽略CO2的溶解和HCl的挥发),则下列分析都正确的组合是

对应图象 | 溶液中的主要成分 | |
A | Ⅰ | NaOH、NaHCO3 |
B | Ⅱ | NaHCO3、Na2CO3 |
C | Ⅲ | NaOH、Na2CO3 |
D | Ⅳ | Na2CO3 |
A. A. B. B C. C D. D
【题目】第四周期过渡元素常与H2O、NH3等形成配合物。
(1)写出Fe元素基态原子的价层电子排布式_______;
(2)C、N、O元素的第一电离能从大到小的顺序为___(用元素符号表示);
(3)向盛有硫酸铜水溶液的试管里加入过量氨水,得到蓝色溶液,铜离子形成了配位数为4的配离子,写出该配离子的结构式为______。
(4)由C、H、O、S中任两种元素构成甲、乙、丙三种分子,所含原子的数目依次为3、4、8,都含有18个电子。甲和乙的主要物理性质比较如下:
熔点/K | 沸点/K | 标准状况时在水中的溶解度 | |
甲 | 187 | 202 | 2.6 |
乙 | 272 | 423 | 以任意比互溶 |
①甲分子的电子式为_________,分子构型为___________;
②1 mol乙分子含有___个σ键;
③丙分子的中心原子采取_______杂化轨道;
④甲和乙的相对分子质量基本相同,造成上述物理性质差异的主要原因是 ____________(结合具体物质解释)。