题目内容
【题目】将等物质的量的Na2CO3、NaHCO3组成的混合物溶于水,配成1L溶液,取出50ml溶液,然后用0. 05mol/L盐酸与它反应,得到图象如下(已知:1mol=1000mmol)
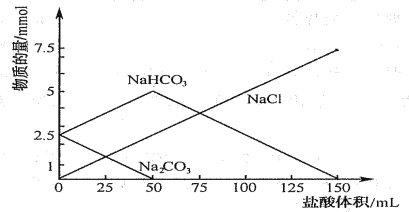
(1)盐酸加到25ml时溶液中发生反应的化学方程式 .
(2)原混合物中Na2CO3物质的量为 mol
(3)盐酸加到150ml时,放出标准状况下气体 mL
【答案】(1) Na2CO3 + HCl = NaCl + NaHCO3;(2) 0.05;(3) 112。
【解析】
试题分析:(1)根据图像,Na2CO3量减少,NaHCO3的量增加,因此发生的反应是Na2CO3+HCl=NaHCO3+NaCl;(2)当加入50mL盐酸时,Na2CO3完全反应,n(Na2CO3)=n(HCl)=50×10-3×0.05mol=2.5×10-3mol,因此1L溶液中n(Na2CO3)=1000×2.5×10-3/50mol=0.05mol;(3)当加入盐酸到150ml,Na2CO3和NaHCO3全部消耗完,NaHCO3全部转化成CO2,消耗盐酸100mL,因此n(CO2)=n(HCl)=100×10-3×0.05mol=5×10-3mol,V(CO2)=5×10-3×22.4×1000mL=112mL。

练习册系列答案
 仁爱英语同步练习册系列答案
仁爱英语同步练习册系列答案 学习实践园地系列答案
学习实践园地系列答案
相关题目