题目内容
【题目】某化学兴趣小组要完成中和热的测定。
(1)实验桌上备有大、小两个烧杯、泡沫塑料、泡沫塑料板、胶头滴管、环形玻璃搅拌棒、0.5 mol·L-1盐酸、0.55 mol·L-1 NaOH溶液,实验尚缺少的玻璃用品是___________、___________。
(2)实验中能否用环形铜丝搅拌棒代替环形玻璃搅拌棒___________(填“能”或“否”),其
原因是 。
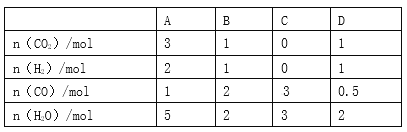
(3)他们记录的实验数据如下:

已知:Q=cm(t2-t1),反应后溶液的比热容c为4.18 kJ·℃-1·kg-1,各物质的密度均为1 g·cm-3。
①计算完成上表ΔH=_____________。
②根据实验结果写出NaOH溶液与HCl溶液反应的热化学方程式: 。
(4)若用KOH代替NaOH,对测定结果__________(填“有”或“无”)影响;若用醋酸代替HCl做实验,对测定结果____________(填“有”或“无”)影响。
【答案】(1)量筒 温度计
(2)否 金属易导热,热量散失多,导致误差偏大
(3)①-56.8 kJ·mol-1②NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l)ΔH=-56.8 kJ·mol-1
(4)无 有
【解析】
试题分析:(1)测定中和热小于用量筒量取酸碱溶液的体积,需要用温度计测量温度,实验尚缺少的玻璃用品是量筒、温度计;(2)金属的导热系数大于玻璃,造成热量散失,误差大,所以不能用金属搅拌器;多次测量,温度取平均值23.4℃,m(HCl) = m(NaOH) = 50g,50 mL0.55 mol·L-1NaOH与50mL.0.5mol·L-1HCl发生中和反应时放出的热量为:Q = Cm(t2 -t1)= 4.18 KJ·℃-1· Kg-1 × 0.1kg × (23.4-20) ℃ = 1.42 KJ,生成1mol水时的反应热为:△H=-1.42 KJ ÷ 0.025 mol = -56.8 KJ/mol。NaOH溶液与HCl溶液反应的热化学方程式:NaOH(aq) + HCl(aq) = NaCl(aq) + H2O(l) ΔH = -56.8 kJ·mol-1。中和热是指在稀溶液中,酸跟碱发生中和反应生成1 mol液态水时所释放的热量,KOH与NaOH同为强碱,故对测定结果无影响;醋酸为弱电解质,溶于水发生电离,放出的热量较小。