题目内容
气体物质A、B、C可发生反应2A(气)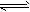 B(气)+xC(气)(已知A的分子量为44)。在1.01×105Pa和2500K时达到平衡状态,在1 mol的A中有0.14 mol分解了,混合气体的密度为0.2g·L-1。则系数的值是
B(气)+xC(气)(已知A的分子量为44)。在1.01×105Pa和2500K时达到平衡状态,在1 mol的A中有0.14 mol分解了,混合气体的密度为0.2g·L-1。则系数的值是
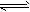 B(气)+xC(气)(已知A的分子量为44)。在1.01×105Pa和2500K时达到平衡状态,在1 mol的A中有0.14 mol分解了,混合气体的密度为0.2g·L-1。则系数的值是
B(气)+xC(气)(已知A的分子量为44)。在1.01×105Pa和2500K时达到平衡状态,在1 mol的A中有0.14 mol分解了,混合气体的密度为0.2g·L-1。则系数的值是 [ ]
A.1
B.2
C.3
D.4
B.2
C.3
D.4
B

练习册系列答案
 浙江名校名师金卷系列答案
浙江名校名师金卷系列答案
相关题目
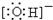
 HCO3-+OH-
HCO3-+OH-