题目内容
某课外活动小组进行Fe(OH)3胶体的制备实验并检验其性质。
(1)若将饱和FeCl3溶液分别滴入下列液体中,能形成胶体的是________。
A.冷水 B.沸水
C.NaOH浓溶液 D.NaCl浓溶液
(2)写出制备Fe(OH)3胶体的化学方程式:____________________________。
(3)怎样用最简捷的方法检验制得的物质是胶体?__________________________ _________________________________________________________________________。
(4)取少量制得的胶体加入试管中,加入(NH4)2SO4溶液,现象是____________________,这种现象称为胶体的______________________。
(5)氢氧化铁胶体稳定存在的主要原因是________。
A.胶体微粒直径小于1 nm B.胶体微粒带正电荷
C.胶体微粒做布朗运动 D.胶体微粒能透过滤纸
(6)Fe(OH)3胶体区别于FeCl3溶液的最本质特征是________。
A.Fe(OH)3胶体微粒的直径在1~100 nm之间
B.Fe(OH)3胶体具有丁达尔现象
C.Fe(OH)3胶体是均一的分散系
D.Fe(OH)3胶体的分散质能透过滤纸
解析: (1)FeCl3在冷水中反应程度小,不能形成Fe(OH)3胶体;FeCl3与NaOH浓溶液反应生成Fe(OH)3沉淀。
(2)书写方程式时不能写成“Fe(OH)3↓”的形式。
(3)丁达尔现象是区别胶体与溶液的最简捷的方法。
(4)Fe(OH)3胶粒所带正电荷被SO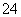 所带负电荷中和,产生红褐色沉淀。
所带负电荷中和,产生红褐色沉淀。
(5)Fe(OH)3胶体稳定存在的主要原因是胶体微粒带正电荷,互相排斥不易形成沉淀;布朗运动是胶体稳定存在的次要原因。
答案: (1)B (2)FeCl3+3H2O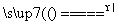 Fe(OH)3(胶体)+3HCl (3)利用丁达尔现象:让一束光线通过制得的物质,从侧面观察到一条光亮的“通路”,说明制得的物质是胶体 (4)产生红褐色沉淀 聚沉 (5)B (6)A
Fe(OH)3(胶体)+3HCl (3)利用丁达尔现象:让一束光线通过制得的物质,从侧面观察到一条光亮的“通路”,说明制得的物质是胶体 (4)产生红褐色沉淀 聚沉 (5)B (6)A

 阅读快车系列答案
阅读快车系列答案已知A(g)+B(g) C(g)+D(g)反应的平衡常数和温度的关系如下:
C(g)+D(g)反应的平衡常数和温度的关系如下:
| 温度/℃ | 700 | 800 | 830 | 1000 | 1200 |
| 平衡常数 | 1.7 | 1.1 | 1.0 | 0.6 | 0.4 |
请回答下列问题:
(1)该反应平衡常数表达式为K=______ ;ΔH 0(选填“>”、“<”或“=”)。
(2)830 ℃时,向一个5 L的密闭容器中充入0.20 mol的A和0.80 mol的B,若测得反应初始至6 S内A的平均反应速率v(A)=0.003 mol · L-1· S-1,则6 S时c(A)=______ mol·L-1;C的物质的量为______ mol 。
(3)在与(2)相同的温度、容器及A、B配比下反应经一段时间后达到平衡,此时A的转化率为______;如果这时向该密闭容器中再充入1 mol氩气,则平衡时A的转化率_ (选填“增大”、“减小”、“不变”)。
(4)判断该反应是否达到平衡的依据为______(填正确选项的字母)。
a.压强不随时间改变 b.气体的密度不随时间改变
c.c(A)不随时间改变 d.单位时间里生成C和D的物质的量相等
(5)1200 ℃时反应C(g)+D(g)  A(g)+B(g)的平衡常数的值为______ 。
A(g)+B(g)的平衡常数的值为______ 。
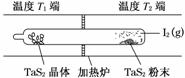
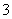 +H+的电离常数Ka=1×10-2 mol·L-1,则该温度下NaHSO3水解反应的平衡常数Kb=________mol·L-1,若向NaHSO3溶液中加入少量的I2,则溶液中
+H+的电离常数Ka=1×10-2 mol·L-1,则该温度下NaHSO3水解反应的平衡常数Kb=________mol·L-1,若向NaHSO3溶液中加入少量的I2,则溶液中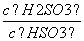 将________(填“增大”、“减小”或“不变”)。
将________(填“增大”、“减小”或“不变”)。