题目内容
下列分子中的碳原子采取sp2杂化的是( )。
| A.C2H2 | B.C2H4 | C.C3H8 | D.CO2 |
B
解析

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列推断正确的是( )
| A.BF3是三角锥形分子 |
B.NH4+的电子式: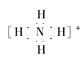 ,离子呈平面形结构 ,离子呈平面形结构 |
| C.CH4分子中的4个C—H键都是氢原子的1s轨道与碳原子的p轨道形成的sp σ键 |
| D.CH4分子中的碳原子以4个sp3杂化轨道分别与4个氢原子的1s轨道重叠,形成4个C—Hσ键 |
有五种元素X、Y、Z、Q、T。X原子的M层上有两个未成对电子且无空轨道;Y原子的特征电子构型为3d64s2;Z原子的L电子层的p能级上有一个空轨道;Q原子的L电子层的p能级上只有一对成对电子;T原子的M电子层上p轨道半充满。下列叙述不正确的是( )。
| A.元素Y和Q可形成一种化合物Y2O3 |
| B.T和Z各有一种单质的空间构型为正四面体形 |
| C.X和Q结合生成的化合物为离子化合物 |
| D.ZO2是极性键构成的非极性分子 |
下列各组物质中,都是由极性键构成的极性分子的一组是( )。
| A.CH4 Br2 | B.H2O NH3 |
| C.CCl4 H2S | D.CO2 HCl |
从键能的角度来看,下列物质中与H2化合时,最难的是( )。
| A.氟气 | B.氮气 | C.氯气 | D.氧气 |
下列对共价键的说法中,不正确的是( )。
| A.共价键是通过形成共用电子对或原子轨道重叠形成的 |
| B.形成共价键的原子之间电负性相同或相差不大 |
| C.一般情况下一个原子有几个不成对电子就会和几个自旋相反的未成对电子成键 |
| D.共价键是通过共用电子对形成的,不属于电性作用 |
已知1 g氢气完全燃烧生成水蒸气时放出热量121 kJ,且氧气中1 mol O=O键完全断裂时吸收热量496 kJ,水蒸气中1 mol H—O键形成时放出热量463 kJ,则氢气中1 mol H—H键断裂时吸收热量为( )。
| A.920 kJ | B.557 kJ | C.436 kJ | D.188 kJ |
下列物质中,含共价键的离子化合物是( )。
| A.MgCl2 | B.N2 | C.HCl | D.Na2O2 |
二氯化二硫(S2Cl2)是广泛用于橡胶工业的硫化剂,其分子结构如图所示。常温下,S2Cl2遇水易水解,并产生能使品红褪色的气体。下列说法错误的是( )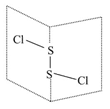
| A.S2Cl2为共价化合物 |
| B.S2Cl2只含有极性共价键 |
| C.S2Cl2与水反应时S—S键和S—Cl键都断裂 |
| D.S2Cl2分子中S—S键和S—Cl键是通过共用电子对的相互作用形成的 |