题目内容
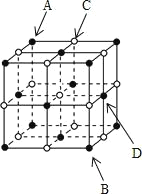
【题目】有固体单质A和淡黄色固体B都能与C反应生成D,同时A与C反应放出单质气体E,B与C反应放出F,E与F在点燃的条件下可以生成C,请回答下列问题:
⑴写出各物质的化学式:
A: ______ B: ______ C: ______D: ______ E: ______ F: ______
⑵写出下列反应方程式:
A与C反应: ______ B与C反应: ______ E与F反应: ______ 。
【答案】Na Na2O2 H2O NaOH H2 O2 ![]()
![]() 2H2+O2
2H2+O2![]() 2H2O
2H2O
【解析】
固体单质A和淡黄色固体B都能与C反应生成D,同时A与C反应放出单质气体E,B与C反应放出F,E与F在点燃的条件下可以生成C,可推知A为Na,B为Na2O2,C为H2O,D为NaOH,E为H2,F为O2。
⑴根据上面分析得出,A:Na,B:Na2O2,C:H2O,D:NaOH,E:H2,F:O2;故答案为:Na;Na2O2;H2O;NaOH;H2;O2。
⑵A与C反应方程式为:![]() ,B与C反应方程式为:
,B与C反应方程式为:![]() ,E与F反应方程式为:2H2+O2
,E与F反应方程式为:2H2+O2![]() 2H2O;故答案为:
2H2O;故答案为:![]() ;
;![]() ;2H2+O2
;2H2+O2![]() 2H2O。
2H2O。

【题目】TiCl4是制备钛及其化合物的重要中间体,可利用下列装置在实验室制备TiCl4(夹持装置略去): TiO2+2C+2Cl2![]() TiCl4+2CO
TiCl4+2CO
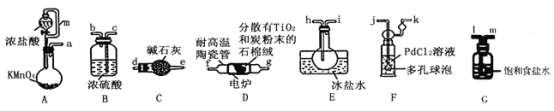
已知:①PdCl2溶液捕获CO时生成Pd单质;②相关数据如下表:
化合物 | 熔点/℃ | 沸点/℃ | 密度/gcm-3 | 溶解性 |
TiCl4 | -25 | 136 | 1.5 | 能溶于有机溶剂:遇水分解生成难溶于水的物质 |
CCl4 | -23 | 76.8 | 1.6 | 难溶于水 |
回答下列问题:
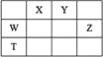
(1)装置A中连通管的作用是______;装置E中使用冰盐水浴的目的是_____________________。
(2)按照气流由左到右的方向,上述装置合理的连接顺序为____________________ (填仪器接口字母);根据完整的实验装置进行实验,实验步骤如下:_____________; 装入药品;向装置A烧瓶中滴加适量浓盐酸,当观察到_________时,加热装置D中陶瓷管;装置E烧瓶中的液体量不再增加时,停止加热,充分冷却。
(3)装置C的作用为___________________。
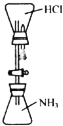
(4)装置F中发生反应的化学方程式为________________________。
(5)制得的TiCl4中常含有少量CCl4, 从混合液体中分离出TiCl4的操作名称为_______________。
(6)利用如图所示装置测定产品纯度:称取w g TiCl4产品进行实验,向安全漏斗中加入适量蒸馏水,待四氯化钛充分反应后,将烧瓶和安全漏斗中的液体一并转入锥形瓶中,用氢氧化钠溶液调节至中性,滴加几滴0.1 molL-1的K2CrO4溶液作指示剂,用cmol L-1 AgNO3标准溶液滴定至终点( Ag2CrO4为红棕色沉淀,可指示滴定终点),重复滴定两次,平均消耗标准溶液V mL。
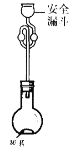
已知:TiCl4 +(2+x)H2O=TiO2xH2O↓+4HCl
①安全漏斗在本实验中的作用除加水外,还有___________。
②根据上述数据计算该产品的纯度为__________。(用含w、c和V的代数式表示)