题目内容
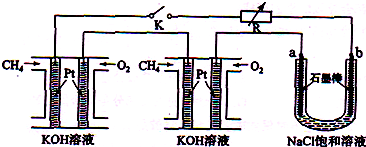
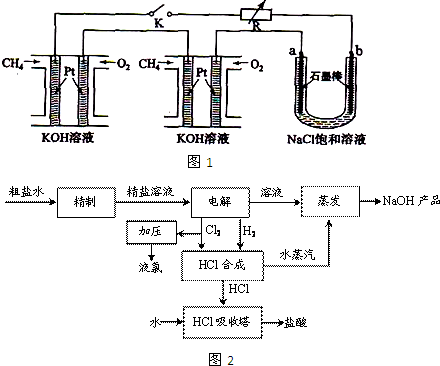
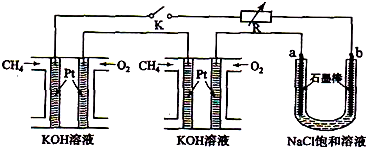
(12分)新型高效的甲烷燃料电池采用铂为电极材料,两电极上分别通入CH4和O2,电解质为KOH溶液。某研究小组将两个甲烷燃料电池串联后作为电源,进行饱和氯化钠溶液电解实验,如图所示:
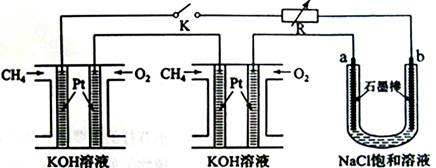
回答下列问题:
(1)甲烷燃料电池正极、负极的电极反应分别为 、 ;
(2)闭合K开关后,a、b电极上均有气体产生,其中b电极上得到的是 ,电解氯化钠溶液的化学方程式为 ;
(3)若每个电池甲烷通入量为1L(标准状况),且反应完全,则理论上通过电解池的电量为
(已知NA=6.02×1023mol-1,电子电荷为1.60×10-19C,列式表示即可),最多能产生的氯气体积为 L(标准状况)。
(1) 2O2 + 4H2O +8e-= 8OH-(2分) ,CH4+10OH--8e-= CO32-+7H2O(2分)
(2)H2
(2分) 2NaCl+2H2O  2NaOH+H2↑+Cl2↑(2分)
2NaOH+H2↑+Cl2↑(2分)
(3) ×8×6.02×1023mol-1×1.60×10-19C (2分) 4L(2分)
【解析】(1)原电池中负极失去电子,正极得到电子,所以甲烷在负极通入,氧气在正极通入,方程式为CH4+10OH--8e-= CO32-+7H2O、2O2 + 4H2O +8e-= 8OH-。
(2)闭合K开关后,b电极和电源的负极相连,作阴极,溶液中的氢离子放电,生成氢气。电解氯化钠溶液的方程式为2NaCl+2H2O
 2NaOH+H2↑+Cl2↑。
2NaOH+H2↑+Cl2↑。
(3)甲烷在反应中失去8个电子,所以电解池的电量为 ×8×6.02×1023mol-1×1.60×10-19C。根据电子得失守恒可知,氯气的体积是 ×8÷2×22.4L/mol=4L。