题目内容
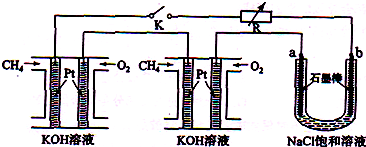
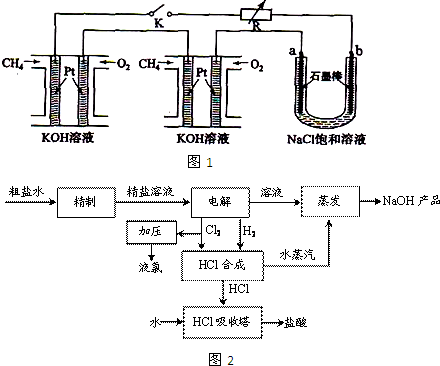
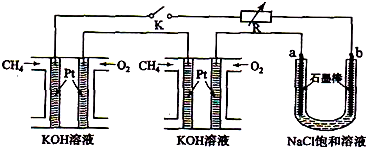
新型高效的甲烷燃料电池采用铂为电极材料,两电极上分别通入CH4和O2,电解质为KOH溶液.某研究小组将两个甲烷燃料电池串联后作为电源,进行饱和氯化钠溶液电解实验,如图所示.回答下列问题:
(1)甲烷燃料电池正极、负极的电极反应分别为
(2)闭合K开关后,a、b电极上均有气体产生.其中b电极上得到的是

(1)甲烷燃料电池正极、负极的电极反应分别为
2O2+4H2O+8e-=8OH-
2O2+4H2O+8e-=8OH-
、CH4+10OH--8e-=CO32-+7H2O
CH4+10OH--8e-=CO32-+7H2O
.(2)闭合K开关后,a、b电极上均有气体产生.其中b电极上得到的是
氢气
氢气
,a电极上所产生气体检验方为法把湿润的淀粉碘化钾试纸靠近a极,若试纸变蓝,说明得到的气体是Cl2
把湿润的淀粉碘化钾试纸靠近a极,若试纸变蓝,说明得到的气体是Cl2
,电解氯化钠溶液的总反应方程式为2NaCl+2H2O
2NaOH+H2↑+Cl2↑
| ||
2NaCl+2H2O
2NaOH+H2↑+Cl2↑
.
| ||
分析:(1)甲烷碱性燃料电池中正极氧气得电子被还原,负极甲烷失电子被氧化;
(2)b连接电源的负极,应为阴极,生成氢气,a连接正极,为阳极,阳极上生成氯气,氯气能使湿润的淀粉碘化钾试纸变蓝色;电解氯化钠溶液生成氢气、氯气和氢氧化钠.
(2)b连接电源的负极,应为阴极,生成氢气,a连接正极,为阳极,阳极上生成氯气,氯气能使湿润的淀粉碘化钾试纸变蓝色;电解氯化钠溶液生成氢气、氯气和氢氧化钠.
解答:解:(1)在碱性溶液中,甲烷燃料电池的总反应式为CH4+2O2+2OH-=CO32-+3H2O,正极是:2O2+4H2O+8e-═8OH-,负极是:CH4-8e-+10OH-═CO32-+7H2O,
故答案为:2O2+4H2O+8e-=8OH-;CH4+10OH--8e-=CO32-+7H2O;
(2)b电极与通入甲烷的电极相连,作阴极,是H+放电,生成H2;a连接正极,为阳极,阳极上氯离子放电生成氯气,氯气能和碘离子发生置换反应生成碘单质,碘与淀粉试液变蓝色,所以检验氯气的方法是:把湿润的淀粉碘化钾试纸靠近a极,若试纸变蓝,说明得到的气体是Cl2;
电解氯化钠溶液的总反应方程式为:2NaCl+2H2O
2NaOH+H2↑+Cl2↑,
故答案为:H2;把湿润的淀粉碘化钾试纸靠近a极,若试纸变蓝,说明得到的气体是Cl2;2NaCl+2H2O
2NaOH+H2↑+Cl2↑.
故答案为:2O2+4H2O+8e-=8OH-;CH4+10OH--8e-=CO32-+7H2O;
(2)b电极与通入甲烷的电极相连,作阴极,是H+放电,生成H2;a连接正极,为阳极,阳极上氯离子放电生成氯气,氯气能和碘离子发生置换反应生成碘单质,碘与淀粉试液变蓝色,所以检验氯气的方法是:把湿润的淀粉碘化钾试纸靠近a极,若试纸变蓝,说明得到的气体是Cl2;
电解氯化钠溶液的总反应方程式为:2NaCl+2H2O
| ||
故答案为:H2;把湿润的淀粉碘化钾试纸靠近a极,若试纸变蓝,说明得到的气体是Cl2;2NaCl+2H2O
| ||
点评:本题涵盖电解池和原电池的主体内容,涉及电极判断与电极反应式书写等问题,做题时注意从氧化还原的角度判断原电池的正负极以及电极方程式的书写,本题中难点和易错点为电极方程式的书写.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目