题目内容
【题目】根据题意填空
(1)有下列八种物质:Br2、I2、KI、K2SO4、KBrO2、H2SO4、KOH、H2O,它们中除一种物质外其余物质是反应物或生成物,已知Br2、I2均为产物,则反应的离子方程式为 .
(2)汽车等的安全气囊强烈碰撞时爆炸,发生的反应如后: 10NaN3+2KNO3=K2O+5Na2O+16N2↑下列判断正确的是
A.每生成8molN2转移15mol电子
B.NaN3中氮元素被还原
C.N2既是氧化剂又是还原剂
D.还原产物与氧化产物质量之比为1:15
(3)某化学兴趣小组希望能较长时间观察到白色絮状 Fe(OH)2的生成,用FeSO4(用铁粉与稀硫酸反应制得)和过量NaOH溶液反应制Fe(OH)2的装置示意图如图所示.回答下列问题: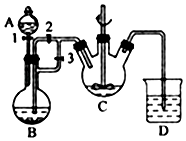
(i)A装置的名称是;在生成Fe(OH)2的装置中,发生的主要反应的离子方程式有
(ii)实验时首先打开活塞3,关闭活塞2,其目的是 .
(iii)若向制得的氢氧化亚铁的容器中通入空气,反应的化学方程式为 .
(iv)若在C中加入的是NH4HCO3时,反应时有气体产生,则最主要的离子方程式将是 .
【答案】
(1)2BrO3﹣+10I﹣+12H+=5I2+Br2+6H2O
(2)D
(3)分液漏斗;H++OH﹣=H2O;Fe2++2 OH﹣=Fe(OH)2↓;排出装置中的空气,防止+2价铁被氧化;4 Fe(OH)2+O2+2 H2O=4 Fe(OH)3;Fe 2++2HCO3﹣=FeCO3↓+CO2↑+H2O
【解析】解:(1)在Br2、I2、KI、K2SO4、KBrO2、H2SO4、KOH、H2O物质中,KBrO2中溴处于高价态,将碘离子氧化成碘单质,反应的离子方程式为:2BrO3﹣+10I﹣+12H+=5I2+Br2+6H2O,所以答案是:2BrO3﹣+10I﹣+12H+=5I2+Br2+6H2O;(2)A.由反应可知,2molKNO3反应转移电子为2mol×(5﹣0)=10mol,即每生成16 mol N2转移10 mol电子,所以每生成8molN2转移5mol电子,故A错误;
B.NaN3中N元素化合价升高,失去电子被氧化,故B错误;
C.只有N元素的化合价变化,则N2既是氧化产物又是还原产物,故C错误;
D.该反应中10molNaN3是还原剂,生成氧化产物N2的物质的量是15mol;2molKNO3是氧化剂,生成还原产物N2的物质的量是1mol,还原产物与氧化产物质量之比为1:15,故D正确;故选D;(3)(i)A装置的名称是分液漏斗;在生成Fe(OH)2的装置中,发生的主要反应氢氧化钠首先中和过量的酸,然后与亚铁离子发生复分解反应生成氢氧化亚铁,所以反应的离子方程式为:H++OH﹣=H2O;Fe2++2 OH﹣=Fe(OH)2↓,所以答案是:H++OH﹣=H2O;Fe2++2 OH﹣=Fe(OH)2↓;(ii)实验时首先打开活塞3,关闭活塞2,是为了排出装置中的空气,防止+2价铁被氧化,所以答案是:排出装置中的空气,防止+2价铁被氧化;(iii)若向制得的氢氧化亚铁的容器中通入空气,反应的化学方程式为4 Fe(OH)2+O2+2 H2O=4 Fe(OH)3 , 所以答案是:4 Fe(OH)2+O2+2 H2O=4 Fe(OH)3
;(iv)若在C中加入的是NH4HCO3时,是碳酸氢根离子与亚铁离子发生双水解,生成二氧化碳气体,离子反应方程式为:Fe 2++2HCO3﹣=FeCO3↓+CO2↑+H2O,所以答案是:Fe 2++2HCO3﹣=FeCO3↓+CO2↑+H2O.

【题目】根据题意填空
(1)根据VSEPR模型判断,下列微粒中所有原子都在同一平面上的一组是 .
A.SO32﹣和NO2﹣
B.NO3﹣和SO3
C.H3O+和ClO3﹣
D.PO43﹣和SO32﹣
(2)CaF2的晶胞如图所示. 
①下列有关CaF2的表达正确的是
a.Ca2+与F﹣间仅存在静电吸引作用
b.F﹣的离子半径小于Cl﹣ , 则CaF2的熔点高于CaCl2
c.阴、阳离子比为2:1的离子化合物,均与CaF2晶体构型相同
d.CaF2中的化学键为离子键,因此CaF2在熔融状态下能导电
②CaF2难溶于水,但可溶于含Al3+的溶液中,原因是(用离子方程式表示,已知[AlF6]3﹣在溶液中可稳定存在).
③晶胞中F﹣的配位数是 , 与一个Ca2+等距离且最近的Ca2+有个.
(3)铜、锌两种元素的第一电离能、第二电离能如表所示
电离能/kJmol﹣1 | I1 | I2 |
铜 | 746 | 1958 |
锌 | 906 | 1733 |
④写出Cu原子核外电子排布式;
⑤铜的第一电离能(I1)小于锌的第一电离能,而铜的第二电离能(I2)却大于锌的第二电离能,其主要原因是 .
【题目】二氧化碳是全球气候变化的主要罪魁祸首,为消除二氧化碳的污染并使其转变为有用物质,全世界的化学科学家做了大量的研究.科学家找到了一种名叫二硒化钨的金属化合物,通过处理,在阳光作用下,使二氧化碳较易分解成一氧化碳和氧气,用一氧化碳可轻松获得多种能源物质.如CO和H2可以合成甲醇.
在10L的密闭容器中按物质的量之比1:2充入CO和H2 , 若充有10molCO发生反应:CO(g)+2H2(g)CH3OH(g).
测得平衡时CO的转化率隨温度变化及压强的变化如图所示: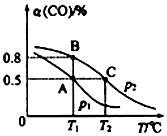
p2、T2时,n(CO)随时间的变化如表所示:
t/min | 0 | 1 | 3 | 5 |
n(CO)/mol | 10 | 7 | 5 | 5 |
(1)p2、T2时,0~lmin 内,平均速率ν(H2)=mol/(Lmin);
(2)你认为p1p2(填“<”“>”或“=”)
(3)合成甲醇的反应为(填“放热”或“吸热”)反应.A、B、C三点的平衡常数KA、KB、KC的大小关系为 .
(4)若工业生产CH3OH,下列措施中,能增加单位时间内CH3OH产量的方法有 .
①增大压强 ②降低温度 ③升高温度
④加入催化剂 ⑤适当增大一氧化碳的比例量 ⑥及时分离CH3OH
(5)己知碳的燃烧热为Q1kJ/mol,碳与氧气反应生成一氧化碳(按量筒整数比)的反应热为﹣Q2J/mol,则二氧化碳在二硒化钨作催化剂时分解的热化学方程式(按最简整数比)为: .



