题目内容
【题目】下列各组离子在指定的溶液中,能大量共存的是( )
①酸性溶液中:Fe2+、Al3+、![]() 、Cl-、I-
、Cl-、I-
②pH=13的溶液:Na+、![]() 、
、![]() 、
、![]() 、S2-
、S2-
③水电离出来的c(H+)=10-13 mol/L的溶液:![]() 、K+、
、K+、![]() 、
、![]()
④加入铝片能放出H2的溶液:Na+、![]() 、Cu2+、
、Cu2+、![]()
⑤滴加石蕊试液显红色的溶液:Fe3+、![]() 、Cl-、
、Cl-、![]()
A.①②B.②③C.②④⑤D.②⑤
【答案】D
【解析】
①酸性溶液中:Fe2+、I-和H+、![]() 发生氧化还原反应,故不符;
发生氧化还原反应,故不符;
②pH=13的溶液:Na+、![]() 、
、![]() 、
、![]() 、S2-不反应,故符合;
、S2-不反应,故符合;
③水电离出来的c(H+)=10-13 mol/L的溶液,可能呈碱性,也可能呈酸性:![]() 在碱性溶液中不共存、
在碱性溶液中不共存、![]() 在酸性溶液中不共存,故不符;
在酸性溶液中不共存,故不符;
④加入铝片能放出H2的溶液,可能呈碱性,也可能呈酸性:![]() 在两种条件下都不能大量共存、Cu2+在碱性条件下不能大量共存,故不符;
在两种条件下都不能大量共存、Cu2+在碱性条件下不能大量共存,故不符;
⑤滴加石蕊试液显红色的溶液,溶液呈酸性:Fe3+、![]() 、Cl-、
、Cl-、![]() 之间不反应,故符合;
之间不反应,故符合;
故选D。

 千里马走向假期期末仿真试卷寒假系列答案
千里马走向假期期末仿真试卷寒假系列答案【题目】下表所列各组物质中,物质之间通过一步反应不能实现如图所示转化的是
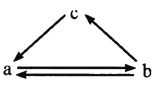
选项物质 | a | b | c |
A | Na2 CO3 | NaHCO3 | CO2 |
B | NO | NO2 | HNO3 |
C | FeCl3 | FeCl2 | Fe |
D | Al2O3 | Al(OH)3 | AlCl3 |
A.AB.BC.CD.D
【题目】一定温度下,在三个体积均为0.5 L的恒容密闭容器中发生反应:CO(g)+Cl2(g)![]() COCl2(g),其中容器Ⅰ中反应在5 min时达到平衡状态。
COCl2(g),其中容器Ⅰ中反应在5 min时达到平衡状态。
容器编号 | 温度/℃ | 起始物质的量/mol | 平衡物质的量/mol | ||
CO | Cl2 | COCl2 | COCl2 | ||
Ⅰ | 500 | 1.0 | 1.0 | 0 | 0.8 |
Ⅱ | 500 | 1.0 | a | 0 | 0.5 |
Ⅲ | 600 | 0.5 | 0.5 | 0.5 | 0.7 |
下列说法中正确的是
A. 容器Ⅰ中前5 min的平均反应速率v(CO)=0.16 mol·L-1·min-1
B. 该反应正反应为吸热反应
C. 容器Ⅱ中起始时Cl2的物质的量为0.55 mol
D. 若起始时向容器Ⅰ加入CO0.8mol、Cl20.8mol,达到平衡时CO转化率大于80%